论文推荐 | 藤茶提取液对红曲菌液态发酵产聚酮类次生代谢产物的影响

藤茶提取液对红曲菌液态发酵产聚酮类次生代谢产物的影响
张德凯1,马文斌1,高梦祥1,*张佳兰2

作者单位
1.长江大学 生命科学学院
2.长江大学 动物科学技术学院
引用格式
张德凯,马文斌,高梦祥,等.藤茶提取液对红曲菌液态发酵产聚酮类次生代谢产物的影响[J].农产品加工,2026,(08):39-43,47.
基金项目
国家自然科学基金面上项目(32372472)



一、引言
藤茶是由葡萄科蛇葡萄属显齿蛇葡萄的茎叶加工成的代用茶,为多年生藤木,春夏之交被白色粉霜覆盖,因此又称白毛猴、莓茶、白毛茶等,主要分布于湖北、湖南、广东等地。藤茶中含有K、Na、Ca等13种矿物质元素,精氨酸、亮氨酸、脯氨酸等17种氨基酸,还有蛋白质、有机酸和膳食纤维等有机成分,黄酮类(二氢杨梅素、杨梅素槲皮素和山奈酚等)、酚类(没食子酸、儿茶素和表儿茶素等)、多糖、甾体(豆甾醇、齐墩果酸和β-谷甾醇等)和挥发油类成分(α-萜品醇、芳樟醇、壬酸、葵酸和桂花醇等)等活性成分。
藤茶中的二氢杨梅素、黄酮和多酚类物质作用主要体现在其药理和功能特性,民间用藤茶泡水来缓解和防治感冒、咽喉肿痛、黄疸性肝炎、高血压、高血脂、皮炎、湿疹等疾病。现代科学研究已经证实,藤茶具有抑菌、祛痰止咳、降血压、降血脂、降血糖、抗炎镇痛、保肝护肝、抗肿瘤和抗癌等作用。
红曲菌(Monascus spp.)是一种腐生丝状真菌,属真菌门、子囊菌亚门、不整子囊菌纲、散囊菌目、红曲科,红曲霉属为红曲科唯一一属。红曲菌的代谢产物丰富,聚酮类次生代谢产物主要有红曲色素、莫纳可林K和真菌毒素-桔霉素等。有研究证明,在橙色红曲菌(Monascus aurantiacus)培养过程中分别添加黄豆苷元、杨梅素和染料木黄酮等9种黄酮类化合物,对桔霉素会产生不同程度的抑制,这可能是与黄酮类化合物的水溶性有关。目前,还没有藤茶影响聚酮类次生代谢产物产生的相关报道。因此,研究在分析藤茶的主要成分的基础上,用藤茶提取液作为外源添加剂,在红曲菌培养过程中添加藤茶提取液,使发酵体系中藤茶黄酮类物质达到一定的浓度,通过测定红曲菌生物量、红曲色素、莫纳可林K和桔霉素的产量,筛选出藤茶提取液的最佳添加量和添加时间,明确藤茶中的黄酮类化合物对红曲菌代谢产物的影响,为藤茶的广泛应用提供理论基础。


二、 材料与方法
(一)材料与设备
紫色红曲菌(Monascus purpureus),长江大学生命科学学院微生物实验室提供;来凤藤茶,购自湖北恩施来凤县;咖啡碱、没食子酸、二氢杨梅素、福林酚,三氯化铝、乙酸钾,上海麦克林生化科技有限公司提供;硝酸钠、磷酸氢二钾、氯化钾、七水硫酸镁、七水硫酸亚铁、蔗糖、葡萄糖、无水乙醇(分析纯)、乙酸乙酯(分析纯),甲醇(色谱纯)、乙腈(色谱纯),国药集团化学试剂有限公司提供。
QXL-1002型程控箱式电炉,上海精宏试验设备有限公司产品;FW100型高速万能粉碎机,天津恒瑞科教仪器有限公司产品;HH-4型数显恒温水浴锅,金坛市杰瑞尔电器有限公司产品;MJ-54A型高压自动灭菌锅、XYQ-LS-50B型系列超纯水机,上海博迅实业有限公司医疗设备厂产品;BS-IE型恒温振荡器,国华电器有限公司产品;UV-2600型紫外分光光度计,岛津企业管理(中国)有限公司产品;DHC-9076A 型电热恒温鼓风干燥箱,上海精密仪器设备有限公司产品;Agilent 1260 型液相色谱高效液相色谱仪,北京京科瑞达科技有限公司产品;FSH-II 型高速电动匀浆机,江苏金坛市环宇科学仪器厂产品。
(二)试验方法
1. 藤茶提取液
干燥藤茶茎叶混合物经粉碎、过筛后,取适量加入蒸馏水,料液比为1∶10(g∶mL),搅匀后静置30 min,沸水浴60 min,每隔10 min搅动1次,使用0.22 μm除菌滤膜过滤,备用。经检测,藤茶提取液中黄酮质量浓度为(11.58±0.93)mg/mL。
2. 主要培养基
1)察氏酵母琼脂培养基(CYA)。NaNO3 3 g,K2HPO4 1 g,KCl 0.5 g,MgSO4·7H2O 0.5 g,FeSO4·7H2O 0.5 g,酵母浸膏5 g,蔗糖30 g,再加入15~20 g琼脂粉,加热溶解后定容至1 L,分装至250 mL锥形瓶中,于121 ℃下灭菌20 min。
2)马铃薯葡萄糖培养基(PDB)。称取200 g洗净去皮的马铃薯,切成小块,加蒸馏水煮烂,用八层干净纱布过滤,加入20 g葡萄糖,定容至1 L,搅拌均匀,分装,自然pH值,于121 ℃下灭菌20 min。
3)马铃薯葡萄糖琼脂培养基(PDA)。在PDB培养基中加入15~20 g琼脂粉,煮沸溶解,定容至1 L后再分装,121 ℃下灭菌20 min。
3. 藤茶主要成分分析
1)水分、灰分、水浸出物、粗纤维和蛋白质的含量均按照国标测定。
2)咖啡碱和茶多酚的含量测定方法及标准曲线的制作按照国标GB/T 8312—2013和GB/T 8313—2018测定。咖啡碱标准曲线回归方程为Y1=0.060 3X1- 0.006 2,R2=0.999 5,X1为咖啡碱质量浓度(μg/L),Y1为波长273 nm处的吸光度;茶多酚标准曲线回归方程为Y2=0.106 1X2+0.014 3,R2=0.998 0,X2为茶多酚质量浓度(mg/L),Y2为波长765 nm处的吸光度。
3)多糖含量测定方法。参照傅宋莉欢等人的方法,略作修改:准确称取2 g,加入50 mL蒸馏水,在80 ℃下水浴1 h,过滤,重复操作1次,合并滤液,定容至100 mL。取10 mL滤液,加入1 mL 5%的苯酚溶液,混合均匀后,缓缓加入5 mL浓硫酸,彻底搅拌,于室温下反应30 min。使用蒸馏水作为参照,于波长490 nm处测定其吸光度。通过标准曲线方程来计算多糖的质量浓度。以葡萄糖为标准品,制作标准曲线,回归方程为Y3=1.323 0X3- 0.057 8,R2=0.993 4,X3为葡萄糖质量浓度(mg/mL),Y3为波长490 nm处的吸光度。
4)黄酮含量测定方法。参照张月荣等人的方法,略作修改:准确称取试样0.5 g,加入体积分数75%乙醇溶液30 mL,置于65 ℃的恒温水浴摇床以转速160 r/min振荡2 h,趁热进行过滤,将滤液收集于50 mL的容量瓶内,接着用乙醇溶液冲洗滤纸和剩余的残渣,将冲洗后的滤液合并。待其冷却至室温后,加水至刻度线,摇晃均匀,得到母液。然后,从母液中取出1 mL,加入水至10 mL容量瓶的刻度线,再次摇匀,备用。
准确吸取待测液1 mL,分别加入三氯化铝溶液2 mL,乙酸钾溶液3 mL,用体积分数75%的乙醇溶液于10 mL容量瓶定容至刻度,摇匀,室温下放置30 min。再以转速4 000 r/min离心10 min,于波长420 nm处测定吸光度,经标准曲线回归方程计算总黄酮含量。以二氢杨梅素作为标准品,制作黄酮标准曲线,回归方程为Y4=29.066X4+0.007,R2=0.999 2,X4为二氢杨梅素质量浓度(mg/mL),Y4为波长420 nm处的吸光度。
4. 红曲菌发酵
取出保存在4 ℃冰箱中的红曲菌试管斜面,将其菌丝接种于CYA斜面培养基,置于30 ℃恒温培养箱中静置培养7 d,使其孢子富集,使用5~8 mL无菌水在无菌环境下洗下孢子,经过3层擦镜纸过滤,得孢子液。使用血球计数板计孢子数,并将孢子悬液以终浓度为1×104个/ mL的接种量加入已灭菌的PDB试管培养基中,置于30 ℃恒温摇床中以转速200 r/min振荡发酵,发酵12 d后检测红曲菌生物量及其代谢物产量。
5. 藤茶提取液添加量和添加时间的确定
分别往PDB培养基中加入不同体积的藤茶提取液,使发酵体系中的藤茶黄酮终质量分数为0.006 25%,0.012 5%,0.025%,0.05%和0.1%,以0为对照组,发酵12 d后检测红曲菌生物量及其代谢物产量。
分别在红曲菌发酵的第2天,第4天,第6天,往培养基中加入藤茶提取液(使发酵体系中藤茶黄酮终质量分数为0.012 5%),以第0天添加为对照组,发酵12 d后检测红曲菌生物量及其代谢物产量。
6. 生物量的测定
红曲菌生物量的测定是参考WAN Y L等人的方法,略作修改,发酵结束后,用擦镜纸过滤发酵液,收集菌丝体,放置于离心管中,加入适量去离子水,充分振荡然后离心(在4 ℃下以转速5 000 r/min离心10 min),弃去上层清水,重复操作3次以清洗菌丝体表面糖类等物质。再放置于60 ℃干燥箱中,干燥至恒质量,称质量。生物量(g/L)是指每单位体积发酵液中的干菌丝体的质量。
7. 色素含量的测定
红曲色素是红曲黄色素(YP)、橙色素(OP)和红色素(RP)这3种不同颜色色素的总称。根据溶解性,又可分为水溶性色素和醇溶性色素。测定方法如下:
将50 mL发酵液置于离心管中,以转速10 000 r/min匀浆2 min,破碎菌体,并与发酵液形成均一的混合液体。取出500 μL混合液体,加入等体积的去离子水,60 ℃下水浴1 h,稀释适当倍数后,得水溶性色素待测样品;吸取300 μL混合液体,加入700 μL无水乙醇,60 ℃下水浴1 h,得醇溶性色素待测样品。水浴结束后冷却至室温,以转速12 000 r/min离心10 min,取上清液稀释适当倍数后于波长410 nm处测得黄色素,波长465 nm处测得橙色素,波长500 nm处测得红色素的吸光度。总色素含量(U/g)的大小表示为每单位质量菌丝体所产生的吸光度,其色价=吸光度×稀释倍数/生物量。
8. 莫纳可林K含量的测定
取500 μL混合均匀的发酵液于1.5 mL离心管中,加入等体积的乙酸乙酯进行萃取,剧烈振荡30 min,以转速12 000 r/min离心10 min,取上清液500 μL 于60 ℃下干燥。再用1 mL苯试剂溶解干燥物,重复上述操作。得到的干燥物用体积分数95%乙醇溶液溶解,稀释适当倍数后,于波长238 nm处测吸光度。莫纳可林K标准曲线回归方程为Y5=0.051X5+ 0.003,R2=0.999 5,X5为莫纳可林K质量浓度(mg/L),Y5为波长238nm处的吸光度。
9. 桔霉素含量的测定
桔霉素含量测定使用高效液相色谱仪(HPLC,Agilent)进行测定,在WAN Y L等人测定方法的基础上稍作修订。吸取发酵液的上清液500 μL至洁净的离心管中,再加入500 μL提前配制好的桔霉素萃取剂混合液(甲苯、乙酸乙酯、甲酸体积比为7∶3∶1,使用前摇匀),剧烈振荡2 min,使其得到充分萃取,以转速12 000 r/min 离心10 min。使用一次性注射器吸取适量上层液,经过 0.45 μm 有机滤膜过滤,去除可能堵塞检测器和色谱柱的杂质,得待测样品。
HPLC条件如下:色谱柱为C18型(5 μm,250 mm×4.6 mm);检测波长为330 nm;流动相为75%乙腈(色谱纯,加入0.05%的三氟乙酸)和25% 的超纯水(加入0.05%的三氟乙酸),其中含有三氟乙酸的超纯水需用0.45 μm 水系滤膜过滤除杂,此外,流动相使用前都需使用超声波仪去除气泡;二极管阵列检测器(Agilent),流速设置为1 mL/min,进样量为20 μL,柱温为30 ℃。
桔霉素标准曲线回归方程为Y6=66.456X6+ 45.782,R2=0.999 7,X6为桔霉素质量浓度(mg/L),Y6为波长330 nm处的吸光度。


三、结果与分析
(一)藤茶主要成分含量
藤茶主要成分含量见表1。
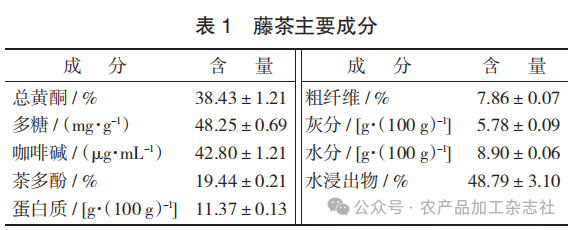
由表1可知,藤茶总黄酮以二氢杨梅素计占比达到了38%,对比报道的显齿蛇葡萄总黄酮在30%~40%,表明试验样品藤茶中总黄酮含量较高。同时,藤茶黄酮含量也受产地、栽培条件、采收期及采收部位等因素的影响。藤茶多糖含量达到了48 mg/g,对比已报道的藤茶中幼嫩茎叶和粗老茎叶的多糖含量为 9.87~10.47 mg/g 和 29.77~30.47 mg/g。表明试验样品藤茶属于粗老茎叶多糖含量高于文献,这可能由于藤茶多糖提取率也随着产地、季节及采摘部位差异有所不同。咖啡碱、茶多酚及水浸出物占比也较高,这也是藤茶由葡萄科蛇葡萄属显齿蛇葡萄的茎叶加工成代用茶的缘由。
(二)添加量对红曲菌次生代谢产物的影响
藤茶提取液添加量对红曲菌液态发酵生物量和聚酮类次生代谢产物的影响见图1。
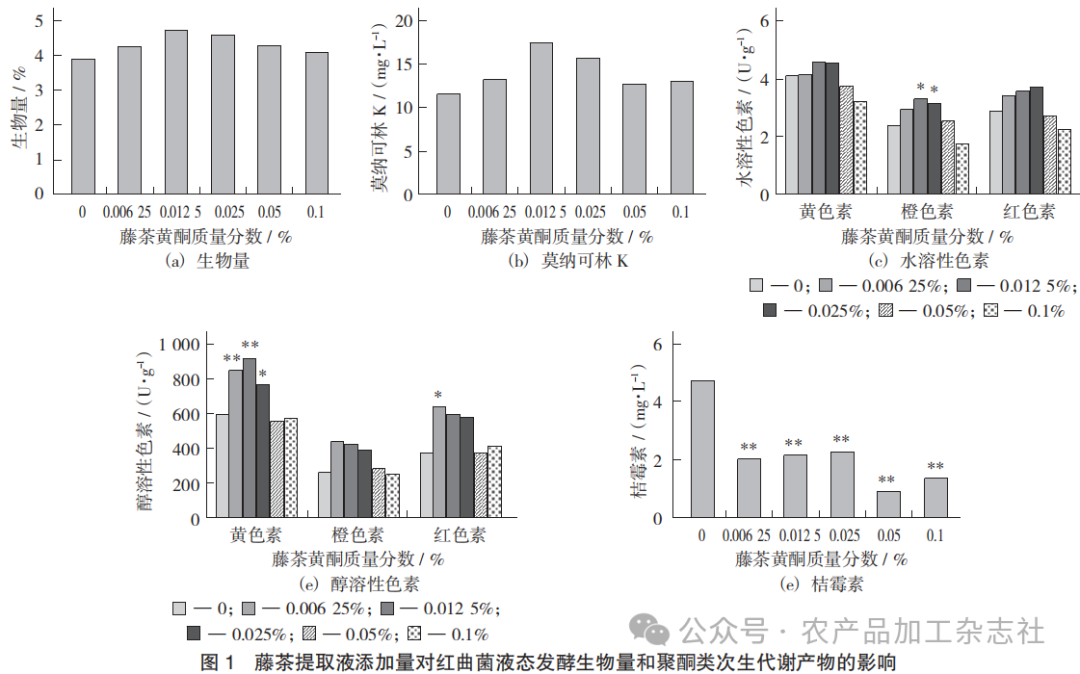
在培养基中添加不同体积的藤茶提取液,使发酵体系中藤茶黄酮质量分数为0,0.006 25%,0.012 5%,0.025%,0.05%和0.1%,发酵12 d,检测红曲菌的生物量、莫纳可林K、红曲色素和桔霉素的含量。0.012 5%和0.025%处理组生物量无显著性差异。莫纳可林K随质量分数由低到高呈先增加后降低的趋势,0.0125%处理组有显著增加,比对照相增加51.15%,表明添加适量的藤茶提取液在不影响红曲菌生长的情况下,有助于莫纳可林K产量的增加。质量分数为0.012 5%和0.025%时,水溶黄色素和水溶红色素的产量均有增加趋势,0.1%处理组均无显著性差异,质量分数为0.012 5%和0.025%时,水溶橙色素比对照组分别增加37.91%和32.41%。醇溶黄色素产量经0.006 25%,0.012 5%和0.025%处理后含量显著增加,比对照组分别增加了43.49%,54.62%和30.37%。各质量分数对醇溶橙色素均无显著作用。0.006 25%使得醇溶红色素比对照组增加69.05%。各质量分数对于红曲菌桔霉素均具有显著抑制作用,质量分数越大,抑制效果就越明显,5个质量分数的处理组与对照组相比分别下降了56.88%,54.02%,51.54%,80.61%,70.46%。综合考虑以上结果,以0.012 5%为藤茶黄酮的最佳添加质量分数。
(三)添加时间对红曲菌次生代谢产物的影响
藤茶提取液添加时间对红曲菌液态发酵生物量和聚酮类次生代谢产物的影响见图2。
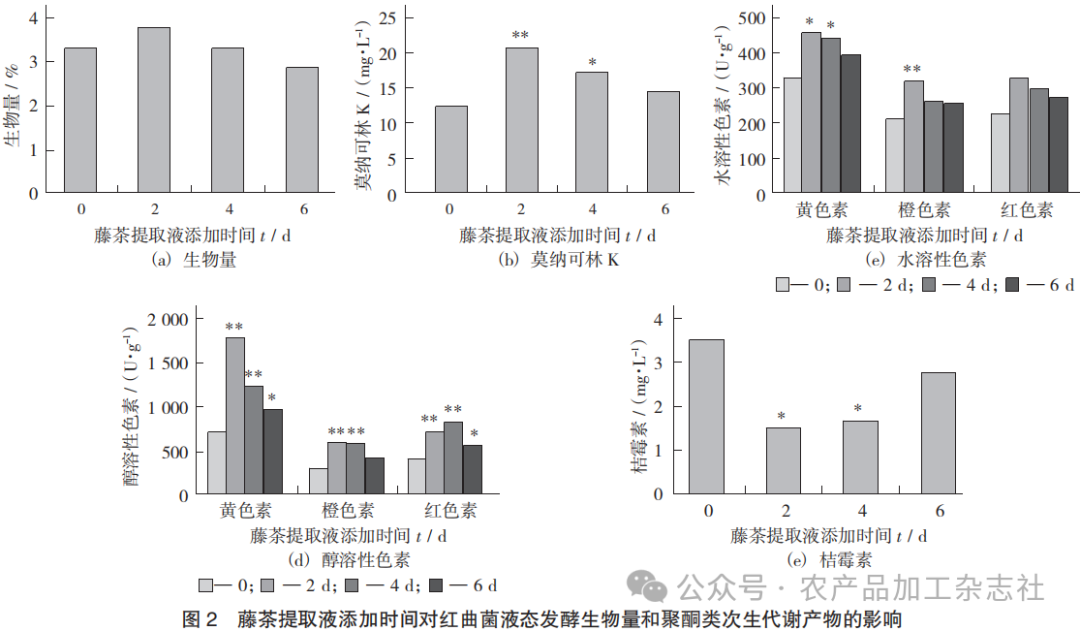
分别在发酵的第2天,第4天,第6天添加藤茶提取液(使发酵体系中藤茶黄酮质量分数为0.012 5%),以第0天添加的为对照组,发酵12 d,检测红曲菌的生物量、莫纳可林K、红曲色素和桔霉素的含量。由图2可知,在第2天添加时,5个处理组均没有显著性差异,说明添加时间对红曲菌生长没有显著影响。第2天和第4天莫纳可林K均有显著差异,比对照组分别增加了68.87%和39.94%。水溶黄色素在第2天和第4天均有显著性增加,与对照组相比分别增加了39.42%和35.22%,第6天没有显著性差异。在第2天添加时水溶橙色素和水溶红色素均有显著性增加,比对照组分别增加了52.35%和44.87%,第4天和第6天均无显著差异。醇溶黄色素和醇溶红色素在第2天,第4天,第6天时均有显著增加,比对照组分别增加了157.32%,75.53%和37.51%;74.20%,103.96%和 37.24%。醇溶橙色素第2天和第4天处理组含量均有显著增加,比对照组分别增加了88.51%和90.89%,第6天没有显著差异。对于桔霉素,在第2天和第4天添加时,均有显著降低,比对照组分别降低了56.74%和51.79%,第6天没有显著差异。
藤茶中的茶多酚具有强抗氧化性,但对真菌抑菌效果不强,且有研究证明,适当浓度的茶多酚对红曲色素的产生具有促进作用,表明了藤茶提取液对红曲菌生物量没有明显影响,但对红曲色素的产生具有明显促进作用。另外,藤茶中的黄酮(主要是二氢杨梅素)对桔霉素的产生具有显著的抑制性,主要是通过二氢杨梅素苯环上的C-OH位点,这个位点是造成桔霉素被还原的关键位点。此外,有研究表明,在红曲菌发酵过程添加染料木黄酮,可影响转运蛋白活性,表明藤茶提取液也可能通过影响红曲菌的蛋白转运过程来影响红曲菌的次生代谢。


四、结论
藤茶主要成分为黄酮(38.43±1.21)%,多糖(48.25±0.69)mg/mL,咖啡碱(42.80±1.21)μg/mL,茶多酚(19.44±0.21)%,水浸出物(48.79±3.10)%。藤茶提取液对红曲菌的生长没有显著影响。在红曲菌发酵第2天添加藤茶提取液,使得发酵体系中藤茶黄酮质量分数为0.012 5%,莫纳可林K产量增加68.87%,水溶性黄色、橙色、红色素产量分别增加了39.42%,52.35%和44.87%,醇溶性黄色、橙色、红色素产量分别增加了157.32%,88.51%和74.20%,桔霉素合成量抑制了56.74%。研究结果表明,添加藤茶提取物可为红曲菌发酵产品的高效安全生产提供有效帮助,为藤茶的综合开发提供了新思路。

编辑:刘 嘉
审核:关 颖
本篇文章刊登于《农产品加工》2026年4期下