论文推荐 | 碱提酸沉法提取红米蛋白工艺优化及功能特性研究

碱提酸沉法提取红米蛋白工艺优化及功能特性研究
李双芳1,2,3,魏雪林1,2,汪慧1,2,王晴雨1,2,
李远远1,2,乔勤勤1,2,*张乐乐1,2

作者单位
1. 阜阳理工学院
2. 阜阳师范大学 信息工程学院
3. 阜阳师范大学 化学与材料工程学
引用格式
李双芳,魏雪林,汪慧,等.碱提酸沉法提取红米蛋白工艺优化及功能特性研究[J].农产品加工,2026,(07):71-76,82.
基金项目
安徽省高校自然科学重点项目(2023AH05852,2024AH051449);安徽省优秀青年教师培育项目(YQYB2024197);安徽省大学生创新创业训练计划项目(S202413619001);安徽省质量工程项目(2023jyxm1023);校级质量工程项目(2022XGJY01)



一、引言
红米起源于中国,是糙米的一种,因色素沉淀在果皮和种皮上而显现出特定颜色,故得此名。目前,红米主要分布在我国福建、广东、广西、江西、云南等地。安徽省阜南县因地处淮河中游北岸,气候温和湿润、土壤肥沃,适合红米种植。据地方志记载,早在汉代,阜南富陂红米就因“色如胭脂、香糯滋补”被列为贡米之一。红米富含脂肪、蛋白质、膳食纤维,以及钙、铁、硒等多种矿物质元素,且整体营养高于普通大米。每100 g红米中含8~9 g蛋白质,高于精白米(6~7 g),且氨基酸组成较为全面、赖氨酸含量较高,弥补了谷物蛋白的短板。此外,红米蛋白可结合膳食纤维,减少胆固醇吸收,辅助降低低密度脂蛋白含量,同时减缓糖分吸收,适宜糖尿病患者食用。除此之外,红米表层色素含有丰富的花色苷、黄酮等生物活性物质,这些成分可与红米蛋白发挥协同作用,清除自由基,延缓细胞衰老。
目前,对于红米的研究主要集中于花色苷、色素、多酚等活性物质,对红米蛋白提取及其应用研究相对较少。植物蛋白的提取方法主要有水提法、盐析法、酸提法、碱提酸沉法等。碱提酸沉法法结合碱溶、酸沉、直接加热法于一体,利用蛋白质在等电点附近发生沉淀的特点,通过调节溶液的pH值使蛋白沉淀,从而得到粗蛋白提取物。该方法工艺简单、操作方便,在植物蛋白提取中应用广泛。试验以富陂红米为原料,优化碱提酸沉法提取红米蛋白的工艺条件,并进一步研究红米蛋白的溶解性、乳化性与乳化稳定性等功能特性,以期为红米蛋白的综合开发利用提供理论依据。


二、材料与方法
(一)材料
富陂红米,安徽省瑞平农业科技有限公司提供;大豆油,金龙鱼食品股份有限公司提供。
(二)试剂
浓硫酸、浓盐酸、硫酸铜、硫酸钾、考马斯亮蓝- G250,均为分析纯,国药集团化学试剂有限公司提供;氢氧化钠、硼酸、95%乙醇、石油醚(30~60 ℃),均为分析纯,西陇科学股份有限公司提供;牛血清蛋白(≥98%),合肥千盛生物科技有限公司提供。
(三)仪器与设备
HYP304型消化炉、KDN103F型定氮仪,上海纤检仪器有限公司产品;JA1003N型电子天平,上海菁海仪器有限公司产品;JB-2型恒温磁力搅拌器、恒温水浴锅,金坛市杰瑞尔电器有限公司产品;722型可见分光光度计,上海佑科仪器仪表有限公司产品;TDZ4-WS型低速自动平衡离心机,上海卢湘仪离心机仪器有限公司产品;DGT-G135型电热鼓风干燥箱,合肥华德利科学器材有限公司产品;PHS-3C型酸度计,上海仪电科学仪器有限公司产品;BJ-800A型多功能粉碎机,永康市天祺盛世工贸有限公司产品。
(四)试验方法
1. 红米脱脂处理
挑选颗粒较饱满、大小均一的红米,粉碎后过60目筛,用石油醚脱脂(红米粉∶石油醚= 1∶5,g∶mL),磁力搅拌2 h,静置12 h,红米粉与上层有机溶剂分离后,倒出有机溶剂进行回收。重复上述脱脂操作1次,最后将红米粉放在通风橱处24 h,使残留的石油醚充分挥发,得到脱脂红米粉,再于30 ℃烘箱中烘干,装入密封袋保存备用。
2. 红米蛋白等电点的测定
称取1 g脱脂红米粉6份,各加入10 mL蒸馏水,使用浓度为0.1 mol/L的NaOH溶液调节pH值至10.0,磁力搅拌10 min使其充分反应,搅拌结束后取上清液,分别用浓度为0.1 mol/L HCl溶液调节pH值至3.0,3.5,4.0, 4.5,5.0,5.5,待蛋白质沉淀后,以转速4 000 r/min离心10 min,分别吸取1 mL上清液,于波长595 nm处测定吸光度,吸光度最小的即为红米蛋白等电点。
3. 红米蛋白的提取
取适量脱脂红米粉过60目筛,按照一定料液比加入蒸馏水,用浓度为0.1 mol/L的NaOH溶液调节溶液pH值,在特定温度下反应一定时间后,以转速4 000 r/min离心15 min,收集上清液。再用浓度为0.1 mol/L的HCl溶液调节上清液pH值至红米蛋白等电点,待蛋白质沉淀后,以转速4 000 r/min离心15 min,收集沉淀,水洗至中性,冷冻干燥即得红米蛋白。
4. 单因素试验
称量1 g脱脂红米粉,通过单因素试验研究料液比、碱提温度、碱提pH值和碱提时间对红米蛋白提取率的影响,试验水平分别选取料液比[1∶6,1∶8, 1∶10,1∶12,1∶14(g∶mL)]、碱提温度(30, 35,40,45, 50 ℃)、碱提pH值(9.0,9.5,10.0, 10.5,11.0)、碱提时间(20,40,60,80,100 min),对碱提酸沉法提取红米蛋白工艺进行初步优化,确定各因素的适宜范围,每个处理重复3次,结果取平均值。
5. 正交试验
在单因素试验基础上,对料液比(A)、碱提温度(B)、碱提pH值(C)和碱提时间(D)进行四因素三水平L9(34)正交试验。
正交试验优化碱提红米蛋白工艺参数见表1。
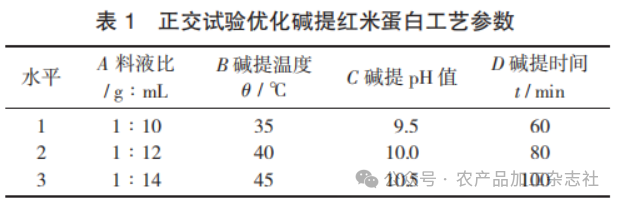
6. 蛋白质含量的测定
红米中蛋白质含量采用《食品安全国家标准 食品中蛋白质的测定》(GB 5009.5—2016)中的凯氏定氮法测定,最终确定红米中粗蛋白为(14.41±1.22)%。提取液中的蛋白质含量采用考马斯亮蓝法进行测定,以牛血清蛋白为标准溶液,以标准牛血清蛋白含量为横坐标(X),以溶液吸光度为纵坐标(Y),绘制标准曲线为Y=0.006 3X+0.127 7(R2=0.998 6)。
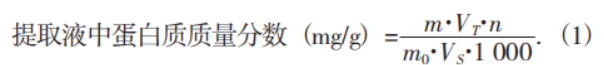
式中:m——根据样品的吸光度从标准曲线计算得到的蛋白质含量,μg;
VT——提取总液体积,mL;
m0——样品质量,g;
VS——测定时取用的样品上清液体积,mL;
n——稀释倍数。
7. 红米蛋白提取率的测定
参照袁梦等人的方法,用上清液中蛋白质质量与原料中蛋白质质量之比来表示。

8. 蛋白质纯度的测定
参照侯玲等人的方法稍作修改,测定提取蛋白质的纯度。

9. 红米蛋白功能性质研究
参照林莉等人方法,稍作修改。研究红米蛋白的溶解性、持水性、持油性、乳化性及乳化稳定性、起泡性及起泡稳定性。
1)溶解性的测定。称取5份0.1 g红米蛋白,分别加入10 mL蒸馏水,用浓度为0.1 mol/L的NaOH溶液和HCl溶液分别调节样品溶液pH值至2.0,4.0, 6.0,8.0,10.0,采用磁力搅拌器搅拌30 min后,再以转速4 000 r/min离心10 min,取其上清液,测定蛋白质含量。

2)持水性和持油性的测定。准确称取1 g红米蛋白粉5份于干燥烧杯中,加入10 mL蒸馏水,分别用浓度为0.1 mol/L的HCl溶液和NaOH溶液调节pH值至2.0, 4.0,6.0,8.0,10.0,不断搅拌呈浆状,倒入离心管以转速4 000 r/min离心10 min,测定上清液体积。
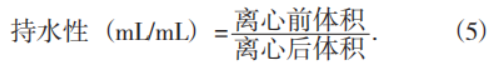
称取1 g红米蛋白在烧杯中,加入10 mL大豆油搅拌1 min,放置室温下静置30 min,记录此时的体积,然后以转速4 000 r/min离心10 min,记录下离心后上清液体积,前后的体积差即为持油性。

3)乳化性和乳化稳定性的测定。配制5%红米蛋白溶液,在室温条件下搅拌使其充分溶解,定容到100 mL容量瓶中,取20 mL的蛋白溶液和5 mL大豆油混合均匀,在涡旋仪中振荡3 min,形成均一的乳化溶液后,以转速4 000 r/min离心10 min。测量离心管中的乳化层体积和液体总体积。
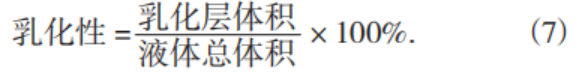
将上述处理好的乳化样品置于80 ℃下水浴30 min,冷却至室温后再次以转速4 000 r/min离心10 min,记录乳化层体积,计算乳化稳定性。

4)起泡性和起泡稳定性的测定。配制质量分数为5%的蛋白溶液,加入100 mL蒸馏水,各取20 mL分别用浓度为1 mol/L的HCl溶液和NaOH溶液调节样品溶液pH值至2.0,4.0,6.0,8.0,10.0,倒入离心管,在高速涡旋仪中振荡3 min,记录此时的液面高度h1,静置30 min后,再次记录此时的液面高度h2。
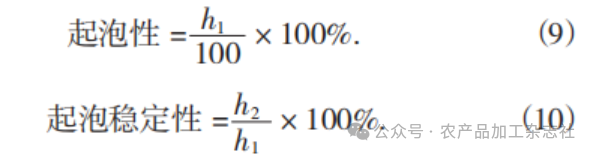
(五)试验数据处理
每组试验重复3次,结果取平均值。单因素试验结果图用Origin Pro 2021软件绘制,显著性分析使用IBM SPSS Statistics 27软件。


三、结果与分析
(一)红米等电点的测定
pH值对蛋白提取液吸光度的影响见图1。
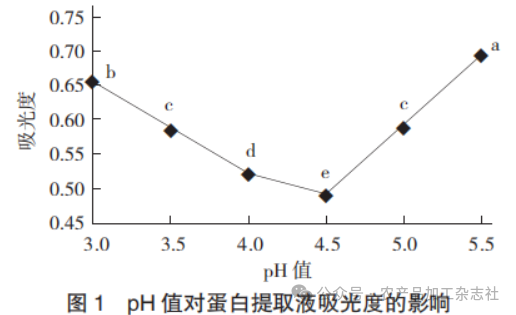
由图1可知,蛋白质上清液的吸光度在pH值3.0~4.5时呈下降趋势,在pH值4.5~5.5呈上升趋势。当pH值为4.5时,吸光度达到最小值,表明该条件下上清液中蛋白质残留量最少,即蛋白质沉淀最多。这主要因为在溶液等电点时,蛋白质溶液中蛋白质的正、负电荷总和为零,蛋白质间的静电排斥作用减弱,从而使蛋白质颗粒之间更易相互碰撞、集聚并形成蛋白质沉淀,由此判断红米蛋白的等电点为4.5,作为酸沉蛋白质的pH值。
(二)单因素试验结果分析
各因素对红米蛋白提取率的影响见图2。
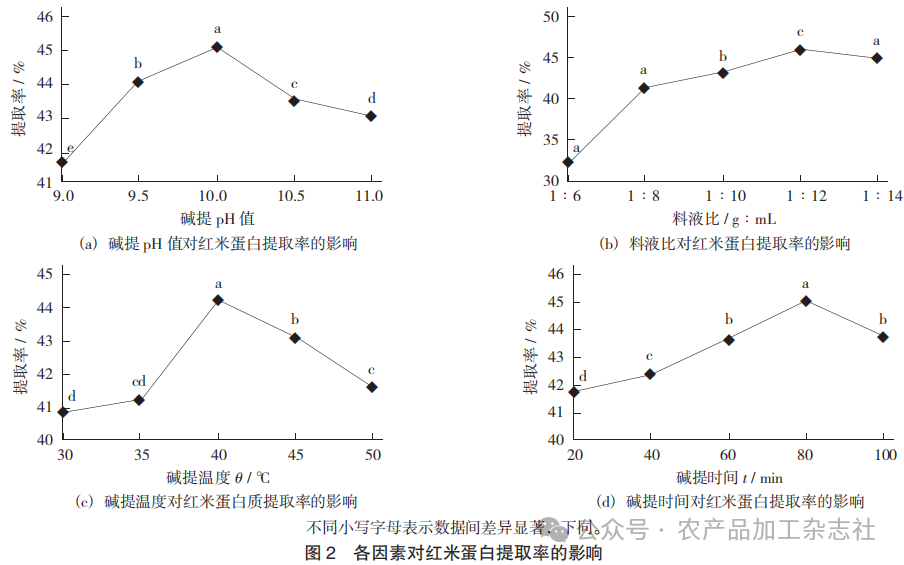
在固定料液比1∶10,碱提温度40 ℃,碱提时间60 min的条件下,考查碱提pH值对红米蛋白提取率的影响。由图2(a)可知,红米蛋白提取率呈先上升后下降的趋势,在碱提pH值为10.0时,红米蛋白提取率达到最高,为(45.07±0.3)%,可能是由于pH值过高会破坏红米蛋白质的空间结构,导致部分蛋白质变性。因此,选取碱提蛋白的最佳pH 值为10.0。
在固定碱提pH值10.0,碱提温度40 ℃,碱提时间60 min的条件下,考查料液比对红米蛋白提取率的影响。由图2(b)可知,料液比为1∶6 ~ 1∶12时,红米蛋白提取率是逐渐升高的;在料液比为1∶12时,红米蛋白提取率达到(45.90±0.58)%。这可能是由于料液比较低时蛋白溶液黏度较大,流动性差,蛋白质溶出速率较小,随着料液比增加,溶液流动性增加,分子扩散速率增强,蛋白质溶出率增加。当料液比为1∶14时,提取率有所下降。因此,选择最佳料液比为1∶12进行后续蛋白质提取优化试验。
在固定碱提pH值10.0,料液比1∶12,碱提时间60 min的条件下,考查碱提温度对红米蛋白提取率的影响。由图2(c)可知,碱提温度从30 ℃上升到40 ℃时,提取率逐渐上升,之后呈下降趋势,可能是因为温度升高,加快了水分子的运动,使得分子间的立体结构伸展,增大了水分子与蛋白质的接触面积,从而加速蛋白质的溶出,但当碱提温度超过40 ℃后,蛋白质分子空间结构会发生改变,蛋白质内部的疏水基团暴露;同时,高温也会导致淀粉糊化,不利于蛋白的分离,从而使红米蛋白提取率降低。因此,选择碱提蛋白最佳温度为40 ℃。
在固定碱提pH值10.0,料液比1∶12,碱提温度40 ℃的条件下,考查碱提时间对红米蛋白提取率的影响。由图2(d)可知,红米蛋白提取率总体趋势呈先升高后降低,当碱提时间达到80 min时,红米蛋白提取率到达最高,为(45.05±0.10)%。随着碱提时间的延长,提取率反而有所下降,一方面可能是随着碱提时间的延长,蛋白质的溶出达到了饱和的状态,所以提取率会有所下降;另一方面随着碱提时间的延长,蛋白质与淀粉结合,导致蛋白质很难析出。因此,选择最佳碱提时间为80 min。
(三)正交试验结果分析
在单因素试验的基础上,以红米蛋白提取率为评价指标,对料液比(A)、碱提温度(B)、碱提pH值(C)和碱提时间(D)进行四因素三水平L9(34)正交试验。
正交试验设计及结果见表2。
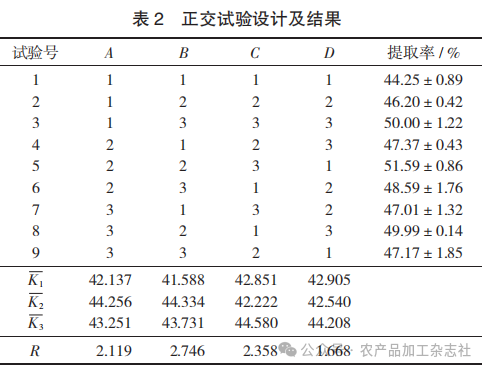
极差分析表明,各因素对红米蛋白提取率的影响主次因素为B>C>A>D,即碱提温度>碱提pH值>料液比>碱提时间;最优提取条件组合为A2B2C3D3,即料液比1∶12,碱提温度40 ℃,碱提pH值10.5,碱提时间100 min。
(四)验证试验
根据正交试验得到最优提取条件进行3次平行试验,得到提取率分别为55.67%,55.63%,56.93%,平均值为(56.08±0.60)%,高于正交试验中任意一组。因此,可确定料液比1∶12,碱提温度40 ℃,碱提pH值10.5,碱提时间100 min,酸沉pH值4.5为红米蛋白的最佳提取工艺。
(五)蛋白质纯度的测定
在最优提取工艺下,测得提取的红米蛋白质纯度为(76.80±0.21)%。
(六)红米蛋白功能性质
1. 红米蛋白的溶解性
pH值对红米蛋白溶解性的影响见图3。
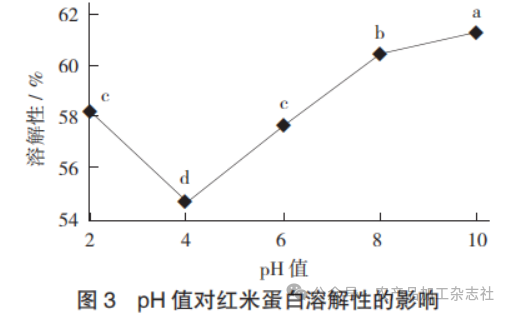

蛋白质的溶解性是蛋白质与水、蛋白质与蛋白质、水与水相互作用的综合结果。当pH值为4时,溶解性降至最低值(54.69±0.21)%,可能是该pH值靠近红米蛋白等电点,致使大部分的蛋白质发生聚沉,使其溶解性降低。随着pH值逐渐升高至碱性范围,蛋白溶解性也不断增大,表明碱性条件下的红米蛋白溶解性要高于酸性条件蛋白的溶解性,这可能与红米蛋白中含有较多的碱溶性蛋白有关。
2. 红米蛋白的持水性
pH值对红米蛋白持水性的影响见图4。
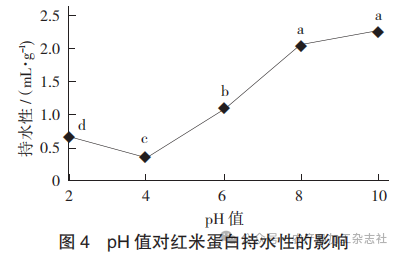

蛋白持水性是指蛋白质结合水分子并能够阻止水渗透的一种能力。由图4可知,随着pH值的变化,持水性呈先下降后上升的趋势,当pH值为4时,持水性降至最低值为(0.35±0.12)mL/g;当pH值在4~10时,持水性逐渐上升,pH值为10时持水性升至(2.25±0.05)mL/g。这可能是因为pH值靠近等电点,蛋白质分子间电荷几乎为零,使得分子间作用力达到最大,蛋白质结合和收缩,呈现出最低的水化和膨胀。随着pH值增大,蛋白质水化和膨胀性能也增大,其持水性能也增强。
3. 红米蛋白的持油性
pH值对红米蛋白持油性的影响见图5。
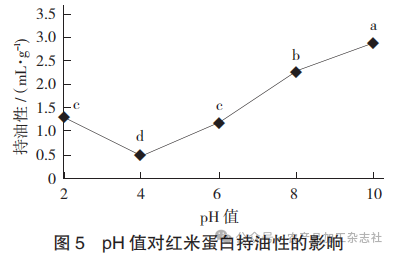
持油性是指蛋白质能够吸附游离脂肪并相结合的能力。由图5可知,持油性随pH值的上升呈现先降低后上升的趋势。当pH值为4时,持油性最低;随着pH值逐渐升高,蛋白持油性也逐渐升高。一方面,可能是pH值接近红米蛋白等电点,蛋白质容易沉淀,使得持油性最小;另一方面,随着pH值的上升,蛋白质结构被破坏,导致内部的非极性键暴露,从而提高与油脂的结合能力,使蛋白质持油性提高,当pH值为10时,持油性升至(2.9±0.1)mL/g。
4. 红米蛋白的乳化性及乳化稳定性
pH值对红米蛋白乳化性及乳化稳定性的影响见图6。
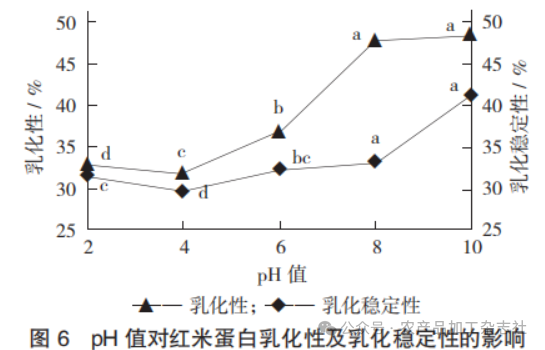
乳化性是指在一定条件下,蛋白质与油、水作用后形成乳浊液的一种能力。乳化稳定性是指当改变外在条件时,蛋白质仍能够维持油水混合不分层的乳化特性的能力。由图6可知,在pH值为4左右时,乳化性及乳化稳定性都是最低的,分别(31.90±0.36)%,(29.89±0.11)%,这是因为在等电点附近溶解性较低,大部分蛋白质都以沉淀的形式存在,不能使溶液吸附在水与油的界面上;随着pH值的升高,蛋白质表面也吸附了较多的负电荷,增大了排斥作用,导致蛋白水化层体积增大,从而提高蛋白乳化稳定性。
5. 红米蛋白的起泡性与起泡稳定性
pH值对红米蛋白起泡性与起泡稳定性的影响见图7。
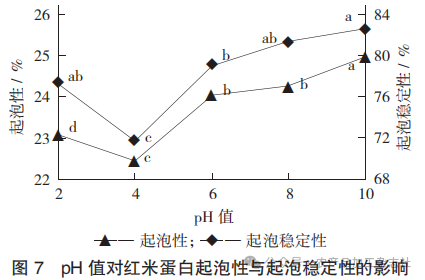
蛋白质的起泡性是指在一定的条件下,蛋白质与水分子和空气形成的一种独特形态混合物的能力。起泡稳定性是指一种能够维持已经形成的泡沫稳定的性能。由图7可知,随着pH值的上升,蛋白起泡性和起泡稳定性都呈现先下降后上升的趋势。已有研究显示,蛋白的起泡性及起泡稳定性与溶解性有着密切的关系,在pH值为4时,起泡性处于最低值(22.45±0.15)%,起泡稳定性达到最低值(71.80±0.03)%;在pH值为10时,起泡性升至(24.96±0.22)%,起泡稳定性升至(82.62±0.12)%。这可能是因为该pH值在等电点的附近,蛋白溶解性较差,起泡性和起泡稳定性相对较差。当pH值增大时,其溶解性也会随之增大,使得蛋白质分子间相互作用力增强,从而更容易形成稳定的气泡,且能维持更长时间。


四、结论
通过单因素试验及正交试验,确定碱提酸沉法提取红米蛋白的最佳工艺为料液比1∶12(g∶mL),碱提温度40 ℃,碱提pH值10.5,碱提时间100 min,酸沉pH值4.5;在该条件下进行验证试验,平均提取率为(56.08±0.60)%,纯度为(76.80±0.21)%。进一步对提取的红米蛋白功能特性进行测定,结果表明pH值的变化对红米蛋白功能性质有很大的影响;当pH值接近红米蛋白等电点时,红米各项功能特性均表现最差;随着pH值的增大,各项功能性质均有不同程度的改善;当pH值为10时,红米蛋白溶解性达到(61.33±0.19)%,同时持水性、持油性及乳化性、乳化稳定性等相应提高,与碎米蛋白功能特性接近。研究为红米蛋白的综合开发利用提供一定的理论依据。

编辑:王裕清
审核:关 颖
本篇文章刊登于《农产品加工》2026年4期上