论文推荐 | 阿拉斯加鳕鱼皮ACE抑制肽的制备及结构鉴定
阿拉斯加鳕鱼皮ACE抑制肽的制备及结构鉴定
袁家琦1,赵彦钦1,李燕苹1,张之凡1,
刘俊松1,王欣颖1,卢 航1,2,田元勇1,2,
王天雨1,2,*赵 慧1,2

作者单位
1.大连海洋大学 食品科学与工程学院;
2.大连工业大学 海洋食品精深加工
关键技术省部共建协同创新中心
引用格式
袁家琦,赵彦钦,李燕苹,等.阿拉斯加鳕鱼皮ACE抑制肽的制备及结构鉴定[J].农产品加工,2026,(05):17-23.
基金项目
国家重点研发计划项目(2024YFD2401904);辽宁省教育厅面上项目(JYTMS20230467)



一、引言
在全球渔业快速发展的背景下,水产品加工过程中产生的大量副产物已成为行业面临的共性难题[1]。传统处理方式多以直接丢弃、廉价饲料化或简易加工为主,导致其中胶原蛋白、生物活性成分等优质资源未得到有效开发[2],这与当前绿色制造和循环经济的发展理念相悖。挖掘水产品副产物的高附加值功能成分,已成为突破产业瓶颈的关键方向[3]。阿拉斯加鳕鱼因营养丰富、肉质鲜美、蛋白质含量高,深受消费者青睐。作为远洋捕捞的重要经济鱼类,鳕鱼被广泛养殖捕捞,并加工成鱼糜及鱼糜制品等[4],但加工产生的鱼骨、鱼鳞、鱼鳍、鱼皮等副产物未被充分利用[5]。鱼皮作为鳕鱼加工的主要副产物,只有少量被二次加工成产品,不仅对环境构成了潜在威胁,同时也造成了资源的极大浪费[6-7]。面对人口增长和食物资源短缺的双重压力,对鱼类加工副产物的综合利用率亟需提高,从水产品加工副产物中提取并生产高附加值产品,可实现资源的有效利用。
鱼皮中含有丰富的蛋白质,蛋白质是由氨基酸通过肽键缩合的生物大分子。许多研究表明,通过一定的技术手段可从各种蛋白质来源的水解物中获得具有特定功能的活性肽[8]。由外源酶促水解制造的食品蛋白酶解产物能够表现出良好的功能性质[9]。ACE抑制肽是一类由10个以下氨基酸残基组成的生物活性寡肽,通过抑制血管紧张素转化酶活性,在血压调节过程中发挥关键作用[10]。以鳕鱼皮为原料,采用酶解工艺制备ACE抑制肽,结合超滤分离、Sephadex LH-20凝胶层析及高分辨液相色谱-质谱联用技术,对酶解产物进行分离纯化与结构鉴定,明确活性肽段的分子结构特征,为食源性降压功能成分的深度开发提供理论依据与试验参考。


二、材料与方法
(一)材料与仪器
阿拉斯加鳕鱼皮,大连市金渤海产食品有限公司提供。
茚三酮,国药集团化学试剂有限公司提供;福林酚,叶源生物技术有限公司提供;血管紧张素转换酶(ACE)、马尿酰组氨酸亮氨酸(HHL),美国Sigma公司提供;LH-20葡聚糖凝胶,北京索莱宝科技有限公司提供。
SYG-2型数显恒温水浴锅,常州朗越仪器制造有限公司产品;TG16-WS型台式高速离心机,湘仪离心机仪器有限公司产品;Synergy HT型多功能酶标仪,美国伯腾仪器有限公司产品;Aglient1260型高效液相色谱仪,安捷伦科技(上海)有限公司产品;RNM-18G型超滤膜,杭州瑞纳膜工程有限公司产品;SCIENTZ-12N型冷冻干燥机,宁波新芝生物科技股份有限公司产品;Lambda 35型紫外分光光度计,珀金埃尔默企业管理(上海)有限公司产品;Triple TOF 7600型高分辨液质联用仪,上海爱博才思分析仪器贸易有限公司产品。
(二) 试验方法
1. 鳕鱼皮酶解液制备工艺流程
鳕鱼皮在-20 ℃下贮藏,试验前先用流水解冻。去除鳕鱼皮残存的鱼肉、鱼鳍和鱼鳞并清洗干净,剪成方块状(2 cm×2 cm),加入浓度为0.1 mol/L 的NaOH溶液,在4 ℃中搅拌24 h,除去杂蛋白。再用去离子水清洗至中性后冷冻干燥,将冻干后的鳕鱼皮在-20 ℃下保存。
2. 蛋白酶的筛选
选用碱性蛋白酶(pH值10,温度50 ℃)、中性蛋白酶(pH值7,温度50 ℃)、木瓜蛋白酶(pH值6,温度50 ℃)、胰蛋白酶(pH值8,温度37 ℃)和胃蛋白酶(pH值2,温度37 ℃)5种蛋白酶对鳕鱼皮进行酶解,并固定料液比1∶40(g∶mL),酶解时间3 h,加酶量3 000 U/g,通过测定鳕鱼皮酶解液的水解度,比较5种酶的酶解情况,确定最适用酶。
3. 水解度的测定
采用茚三酮法[11]测定水解度。
凯氏定氮法测定氮含量,并根据公式(1)计算水解度(DH)。 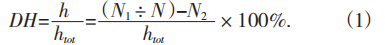
式中:h——水解后每克蛋白质被裂解的肽键毫摩尔数;htot——每克原料蛋白的肽键毫摩尔数;N1——水解液中氨基的浓度,mmol/mL;N——水解后水解液中蛋白质量浓度,mg/mL;N2——原料蛋白中游离氨基浓度,mmol/g。
4. 单因素试验
选取酶解时间(A)、料液比(B)和加酶量(C)进行单因素试验,以水解度为指标,研究各因素对鳕鱼皮酶解液水解度的影响。
5. 正交试验
以单因素试验结果为基础,研究各因素对鳕鱼皮酶解液水解度的影响,设计正交试验表,探究酶解鳕鱼皮的最佳工艺条件。
正交试验因素与水平见表1。

6. ACE抑制率的测定
参照TU M等人[12]的方法进行改动并测定。将5 mL样品溶液与25 mL HHL溶液混合,在37 ℃下保温10 min,加入20 mL ACE溶液,在37 ℃下反应1 h后加入浓度为1 mol/L的盐酸溶液20 mL终止反应,充分涡旋,再加入150 mL超纯水(0.1 mol/L硼酸盐缓冲液代替样品作为空白组)。反应后的溶液经0.22 mm针头滤膜过滤除杂,并用高效液相色谱仪进行检测。
色谱条件:流动相A、B和C分别为甲醇溶液、超纯水(含0.1%的FA)和乙腈,Hypersil BDS C18型色谱柱,柱温25 ℃,流速1 mL/min,进样量20 mL,检测波长228 nm。
根据公式(2)进行ACE抑制率的计算。 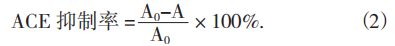
式中:A0——空白组马尿酸峰面积;
A——样品组马尿酸峰面积。
7. 超滤分离
用截留分子量分别为30,10,6 ku的超滤膜对鳕鱼皮ACE抑制肽(CSCP)进行超滤分离。将收集到的4个组分分别命名为CSCP-1(Mw>30 ku)、CSCP-2(30 ku>Mw>10 ku)、CSCP-3(10 ku>Mw> 6 ku)和CSCP-4(Mw<6 ku),冷冻干燥。
8. 葡聚糖凝胶层析分离
参考HUO J X等人[13]的方法,选用Sephadex LH- 20作为分离的凝胶层析介质。将凝胶煮沸活化后,用玻璃棒将凝胶缓慢引入层析柱中,待凝胶自然沉降后,用5倍柱体积的30%甲醇溶液将层析柱压实后上样,连接恒流泵进行洗脱。使用自动部分收集器收集洗脱液,重复进样,多次收集,用紫外分光光度计在波长280 nm处测定吸光度,绘制洗脱曲线,旋转蒸发除去甲醇后进行冷冻干燥。
9. 液质联用鉴定
将样品以0.1%(V/V)的FA-H2O复溶,样品质量浓度为0.2 mg/mL,进样量为400 ng。预处理柱C18型Micro Trap 10×0.3 mm,3/pk,分析柱:Kinetex 2.6 μm XB C18型100A LC Column 150×0.3 mm。串联质谱以正离子数据依赖模式采集获取,质谱扫描设定为一个全扫描质荷比(m/z)范围350~1 250的离子,累积动态时间0.25 s,并对其中最强的40个离子进行离子碰撞解离(CID),再进行MS/MS扫描,质荷比扫描范围100~1 500,累积动态时间0.05 s;使用Waters ACQUITY UPLC M-Class运输流动相,用Mascot 2.4.1软件在阿拉斯加鳕鱼蛋白数据库中进行检索。
(三)数据处理
所有样品平行测定3次,用SPSS 17.0统计软件对结果进行统计分析来评估显著性差异水平p<0.05,用Excel 2010软件作图。


三、结果与分析
(一)蛋白酶的筛选
在酶解过程中,蛋白酶种类是影响水解产物特性的关键因素[14]。不同种类蛋白酶因其独特的空间构象和催化特性,在底物特异性及酶切位点等方面存在显著差异[15]。
蛋白酶种类对水解度的影响见图1。
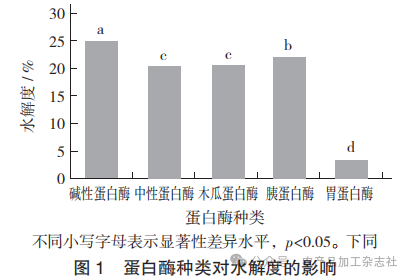
由图1可知,碱性蛋白酶展现出最优的水解性能,其水解度达到(24.73±0.42)%,优于胰蛋白酶的水解度(21.97±0.18)%(p<0.05)、木瓜蛋白酶的水解度(20.50±0.20)%(p<0.05)、中性蛋白酶的水解度(20.34±0.45)%(p<0.05)和胃蛋白酶的水解度(3.31±0.18)%(p<0.05)。这可能归因于碱性蛋白酶的活性中心含有丝氨酸残基,能够有效识别蛋白中的疏水性氨基酸残基,特别是对芳香族氨基酸和脂肪族氨基酸的羧基端具有高度特异性切割能力[16]。
(二)单因素试验
1. 酶解时间对水解度的影响
选用0~5 h作为酶解时间的水平因素进行单因素试验。
酶解时间对水解度的影响见图2。
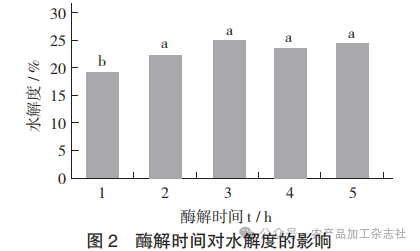
酶解时间决定了酶解程度是否充分,时间过短则不能充分发挥蛋白酶的功效,时间过长则会造成过度酶解。由图2可知,在其他因素固定,酶解时间在1~5 h内,水解度呈先上升后平稳的趋势,在3 h时达到最高值(24.70±0.63)%。分析其原因可能是由于在0~2 h内,蛋白酶的活性位点充分暴露,与底物能够足够反应,有利于酶解的传质过程。当反应进行至3 h时,蛋白酶与底物的接触接近饱和,多数蛋白与酶结合的活性位点已被切割,可酶解的肽键变少,无法水解出更多肽段,且伴随着游离肽对产物的抑制不断增加,也导致水解度不再大幅变化。因此,选取3 h作为酶解鱼皮的最佳酶解时间。
2. 加酶量对水解度的影响
设置加酶量分别为750,1 500,2 250,3 000, 3 750,4 500 U/g,在酶解时间3 h,料液比1∶40,酶解温度和pH值均为酶的最适条件下进行试验。
加酶量对水解度的影响见图3。
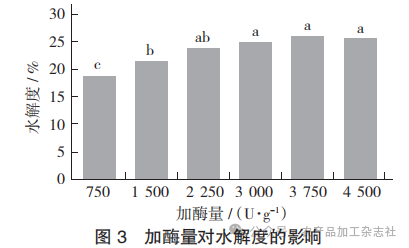
由图3可知,加酶量在750~3 000 U/g内,水解度呈逐渐上升趋势,原因是随着酶浓度的提高,溶液中酶活性基团增加,可充分与底物结合,导致底物蛋白被不断水解,提高了酶解效率;当加酶量为 3 000 U/g时,水解度保持相对稳定的水平,达到(24.87±1.50)%;当加酶量超过3 000 U/g时,水解度较稳定且无显著性差异,推测底物与酶的结合已达到饱和,过剩的酶不再与底物发生反应,酶解产物不再释放,即使再加入更多蛋白酶,水解度也不再大幅增加,反而造成浪费。因此,选择3 000 U/g的加酶量作为最佳试验条件。
3. 料液比对水解度的影响
设置料液比分别为1∶20,1∶30,1∶40,1∶50,1∶60,在酶解时间3 h,加酶量3 000 U/g,酶解温度和pH值均为酶的最适条件下进行试验。
料液比对水解度的影响见图4。
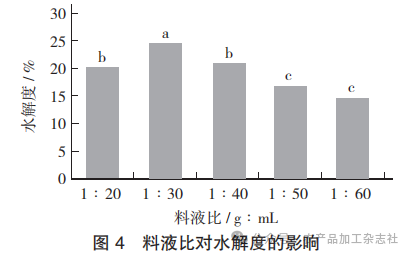
由图4可知,当料液比为1∶30 时,水解度达到最高值为(24.50±1.27)%;随着料液比的增加,水解度呈下降趋势,分析其原因可能是随着酶的有效浓度降低,无法再与靶点接触,酶解效率降低,底物蛋白不再高效被酶解,从而造成了水解度的下降[17]。因此,选择料液比1∶30 作为最佳试验条件。
(三)正交试验结果及分析
根据单因素试验结果,考查酶解时间(A)、料液比(B)和加酶量(C)对酶解产物水解度的影响,进行三因素三水平正交试验,确定最佳酶解条件。
正交试验结果见表2。
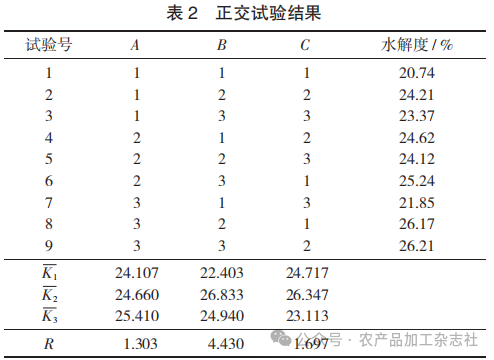
根据各因素极差项R值可知,各因素对酶解产物水解度影响程度的顺序为料液比(B)>加酶量(C)> 酶解时间(A);根据各因素水平对应的平均值K,最优组合为A3B2C2,即最佳酶解工艺为酶解时间4 h,料液比1∶30,加酶量3 000 U/g,此时水解度能够达到(28.00±0.25)%,该条件下的鳕鱼皮酶解液ACE抑制活性为(63.20±1.39)%,说明其具有ACE抑制活性。
(四)超滤分析
超滤是一种常用于分离不同分子量多肽的技术。通常来说,多肽的分子量与其生物学活性有着紧密联系,低分子量的肽类在ACE抑制活性方面表现得更为显著[18]。
超滤各组分ACE抑制活性见图5。
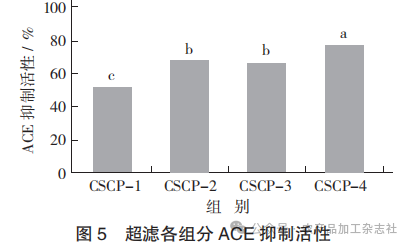
由图5可知,CSCP经超滤分离后得到CSCP-1、CSCP-2、CSCP-3和CSCP-4这4个组分。CSCP-4的ACE抑制活性最高,达到(76.61±1.41)%,IC50值为(0.79±0.06)mg/mL。这与LIN L等人[19]探究鱿鱼皮明胶水解物的ACE抑制活性相似,Mw<2 ku的组分ACE抑制活性明显高于10 ku>Mw>6 ku组分。这类结果的出现可能源于ACE酶活性中心的槽形结构。由于高分子量肽的空间折叠更为复杂,使其难以接近活性中心位点;相反,低分子量肽则能更容易抵达ACE的活性中心位点,从而减缓酶促反应的速度,增强其抑制效果[20]。此外,CSCP-4的ACE抑制活性也高于CSCP,这表明超滤技术能够有效富集出高活性的抑制肽。
(五)葡聚糖凝胶LH-20层析分离
葡聚糖凝胶(Sephadex)是一种基于交联葡聚糖基质构建的三维网状球型凝胶材料。当含有多肽混合物的溶液流经层析柱时,低分子量组分进入凝胶内部微孔,其移动路径需穿过连续的网状孔隙结构;而高分子量物质无法进入凝胶内部微孔,仅能沿凝胶颗粒间空隙形成的流体通道移动。基于此差异,大分子物质在流动相驱动下优先穿过柱床,实现分离,而小分子物质因受内部孔隙阻碍呈现延迟洗脱,而后被分离出来[21]。将超滤后ACE抑制活性最高的CSCP-4样品通过Sephadex LH-20层析柱进行分离。
Sephadex LH-20分离CSCP-4各组分见图6,CSCP- 4D经Sephadex LH-20分离各组分的ACE抑制活性见图7。
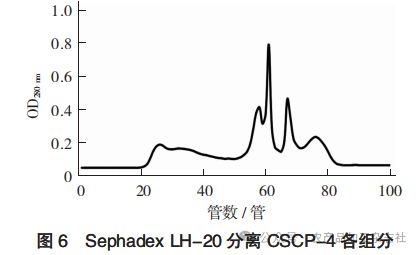
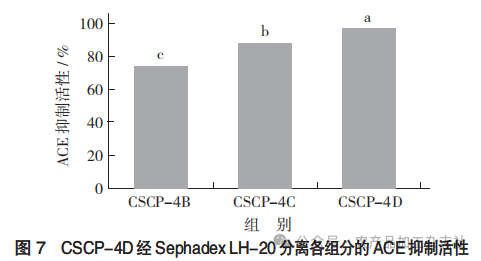
由图6可知,共分离出4个峰,分别命名为CSCP- 4A、CSCP-4B、CSCP-4C和CSCP-4D。由于CSCP- 4A的分离效果不佳,只测定了CSCP-4B、CSCP-4C和CSCP-4D的抑制活性。由图7可知,经测定,CSCP-4B、CSCP-4C和CSCP-4D的ACE抑制活性分别为(73.53±3.68)%,(87.05±1.80)%,(96.16± 0.54)%。其中,CSCP-4D具有最强的ACE抑制活性,其IC50值为(0.22±0.01)mg/mL,选择CSCP- 4D进行后续的纯化。
(六)ACE抑制肽结构的确定
对Sephadex LH-20分离后ACE抑制活性最高的CSCP-4组分进行LC/MS鉴定分析。
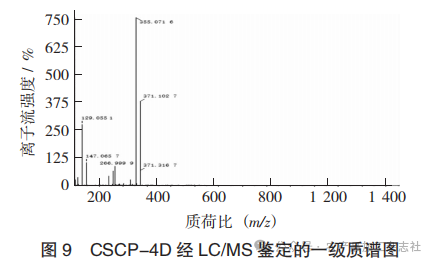
CSCP-4经LC/MS鉴定的总离子峰图见如图8,CSCP-4D经LC/MS鉴定的一级质谱图见图9。
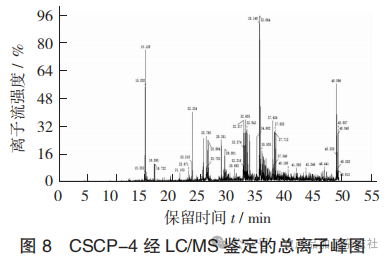
通过与阿拉斯加鳕鱼数据库进行对比,共鉴定出29条多肽结构。
液质联用鉴定的多肽结构见表3。
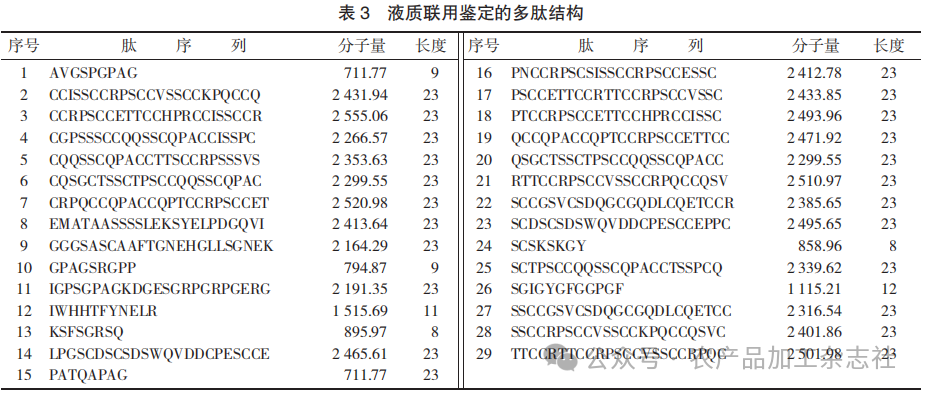
根据质谱图显示的母离子质荷比为371.3 u,结合对比蛋白库的结果信息。首先,考虑母离子的电荷状态,可能的电荷数包括单电荷、双电荷或三电荷,因为单电荷对应的肽段太短,不符合常规酶解产物的长度,所以优先考虑是双电荷或三电荷的可能性较大。然后,根据分子量的计算推断该物质可能是带有三电荷的SGIGYGFGGPGF肽链。SGIGYGFGGPGF的分子量为1 114.51 u,当携带三电荷时质荷比约为371.5,与母离子质荷比的差异仅有0.2 u,该数值在试验误差范围内。此外,该肽段的可信度指标PEP值为2.98×10-8,且Score值为50.607,能够说明匹配度较好。同时,对碎片离子信息进行查看,质谱图中的碎片离子峰如质荷比129.055 1,147.065 7,266.999 9和355.071 6,需与SGIGYGFGGPGF的理论碎片进行对比,SGIGYGFGGPGF的序列可能产生GYGFGGPGF等碎片,对应质荷比理论值为267.13,与266.999 9非常接近。对SGIGYGFGGPGF的特征进行分析,其长度为12个氨基酸,含有多个甘氨酸(G)和苯丙氨酸(F),GFGGPGF的重复模式是胶原蛋白Gly- X-Y模式的典型特征,能够形成稳定构象。关键氨基酸酪氨酸Tyr(Y)位于第5位,可能参与疏水相互作用,苯丙氨酸Phe(F)位于C端的第1位,脯氨酸Pro(P)位于C端第3位,符合ACE抑制肽的C端偏好。文献报道,C端三肽序列含有疏水性氨基酸(Phe、Trp、Tyr、Val、Leu和Ile)时有利于ACE抑制活性的提高[22],C端含有脯氨酸Pro(P)的肽具有更高的ACE抑制活性,C端第2位为甘氨酸Gly(G)能够提供柔软的韧性,利于结合。综上所述,SGIGYGFGGPGF与质谱图母离子高度吻合。基于上述质谱分析与序列特征的理论推断,后续需针对SGIGYGFGGPGF开展实际ACE抑制活性验证,以明确其功能价值。活性验证不仅能夯实“结构-活性”关联的科学性,更能为该肽在功能食品、生物医药领域的开发提供关键试验依据,推动从质谱表征到实际应用研究闭环。


四、讨论
以阿拉斯加鳕鱼皮为原料,通过单因素试验及正交试验优化得出鳕鱼皮酶解液的最佳制备工艺为酶解时间 4 h,料液比 1∶30(g∶mL),加酶量 3 000 U/g,此时水解度最大达(28.00±0.25)%,ACE 抑制活性为(63.20±1.39)%,证明其具有ACE抑制活性;利用超滤分离、葡聚糖凝胶层析分离和高分辨液质联用仪对鳕鱼皮 ACE 抑制肽进行分离纯化及成分鉴定,通过分子量的计算推测SGIGYGF- GGPGF序列与质谱鉴定结果高度吻合,后续将对该十二肽进行活性及作用机理的深入探讨;初步鉴定出具有 ACE 抑制活性的成分,为从水产品加工副产物中挖掘降压活性成分提供了新的思路。

编辑:谷金星
审核:关 颖
本篇文章刊登于《农产品加工》2026年3期上