论文推荐 | 肽参牡蛎饮的特性分析及功能评价
肽参牡蛎饮的特性分析
及功能评价
何嘉怡1,陆 伟1,张松姿1,
晏永球1,王 俊1,贾福怀1,2

作者单位
1.宁波御坊堂生物科技有限公司;
2.浙江大医德美生物科技有限公司
引用格式
何嘉怡,陆伟,张松姿,等.肽参牡蛎饮的特性分析及功能评价[J].农产品加工,2026,(04):25-28.
基金项目



一、引言
随着现代社会生活节奏加快和年龄增加,下丘脑-垂体性腺轴功能逐步减退,促性腺激素释放激素分泌下降,造成性功能减弱等症状。流行病学调查表明,40~70岁男性性功能障碍的总体患病率可达50%以上,其致病因素复杂,涉及器质性病变、不良生活方式及精神心理与医源性因素等多重维度[1]。目前,临床一线治疗以西药为主,其中5型磷酸二酯酶抑制剂凭借其确切的疗效占据主导地位。然而,此类药物存在头痛、面部潮红、视觉异常等特定副作用,且仅为对症治疗,无法从根本上改善机体功能,同时存在心血管风险患者用药禁忌等局限性[2]。在此背景下,功能食品的研发是极具潜力的方向,其中食源性低聚肽作为研究热点,已发现如牡蛎肽等代表性成分。有研究证实,牡蛎肽能增强TM3细胞增殖活力、促进雄性激素生成[3-4],对性功能具有改善作用。
当前,基于TM3细胞的性功能评价模型存在局限性。主流研究多以处于正常生理状态的细胞作为研究对象[3-6],并将睾酮产出量作为单一的终点评价指标。此种范式存在以下核心问题:首先,其未能模拟与年龄相关性功能减退或代谢性疾病相关的病理生理状态(如氧化应激、慢性炎症等)[7],从而削弱了其与人类主要临床需求的关联性。更为重要的是,该模型将睾酮合成过程视为一个“黑箱”,忽视了其与线粒体能量代谢、氧化还原稳态及细胞炎症网络等关键上游调控通路的有机联系,从而严重制约了高效、安全的功能因子筛选与产品开发进程。
以氧化应激诱导的功能受损小鼠睾丸间质细胞(TM3细胞)为模型,探究了肽参牡蛎饮对线粒体功能、睾酮合成及氧化还原平衡的关键调控作用。通过上述细胞水平的机制解析,阐明了肽参牡蛎饮提升雄激素水平的内在机制,为其作用原理提供了试验依据,也为同类功能饮品提供了一种基于细胞水平的评价途径。


二、材料与方法
(一)仪器与设备
YC-1000A2型生物安全柜,苏州苏信环境科技有限公司产品;DIGICEN21 R型冷冻离心机、WCI- 260型二氧化碳培养箱,维根技术(北京)有限公司产品;NIB-620FL型荧光倒置显微镜,宁波永新光学股份有限公司产品;Varioskan LUX型多功能酶标仪,赛默飞世尔科技公司产品;A388型全自动氨基酸分析仪,德国曼默博尔公司产品。
(二)主要试剂
肽参牡蛎饮,宁波御坊堂生物科技有限公司提供;TM3细胞,赛百慷(上海)生物技术股份有限公司提供;DMEM/F12培养基、胎牛血清、马血清,美国Gibco公司提供;青霉素-链霉素溶液(100×)、PBS磷酸盐缓冲溶液(1×)、胰酶细胞消化液(0.25%胰酶,含EDTA,不含酚红),北京兰杰柯科技有限公司提供;CCK-8型细胞活力检测试剂盒、超氧化物歧化酶(SOD)测定试剂盒、细胞丙二醛(MDA)测定试剂盒、睾酮(TESTO)测试盒、双氢睾酮测定试剂盒,南京建成生物工程研究所提供;JC-1型线粒体膜电位检测试剂盒,上海碧云天生物技术有限公司提供。
(三)试验方法
1. 牡蛎肽氨基酸组分分析
依据《食品安全国家标准 食品中氨基酸》(GB 5009.124—2016)的测定方法,采用全自动氨基酸分析仪对牡蛎肽中的氨基酸组成进行测定。
2. TM3细胞培养
将TM3细胞接种于DMEM/F12完全培养基(含2.5%胎牛血清、5%马血清、1%双抗)中,置于37 ℃培养箱中培养。待细胞贴壁生长至80%的融合度时,弃培养液,用PBS溶液轻轻润洗细胞,用胰蛋白酶消化并以1∶3比例进行传代。试验均使用处于对数生长期状态良好的细胞。
3. CCK-8法检测肽参牡蛎饮对TM3细胞增殖率的影响
取TM3细胞以1×105个/ mL接种于96孔培养板中,每孔100 μL,培养24 h。试验组加入不同体积分数(5%,10%,15%)的肽参牡蛎饮,每个体积分数设置3个复孔,同时设置对照组(完全培养基+细胞),培养48 h后每孔加入10 μL CCK-8溶液,避光孵育40 min后于波长450 nm处测定吸光度,计算细胞活力。
4. 分组及氧化应激模型建立
向12孔板加入1×105个/ mL的TM3细胞悬液,每孔0.5 mL,培养24 h。分为空白对照组、氧化应激模型组、试验组,试验组细胞给予0.5 mL 体积分数5%的肽参牡蛎饮,空白对照组与氧化应激模型组细胞给予0.5 mL DMEM/F12完全培养基,培养48 h。孵育结束后,除空白对照孔外,其余孔均需进行400 μmol/L H2O2诱导,诱导时间为2 h。
5. 抗氧化水平检测
1)胞内ROS水平检测。取1.3.4中各组细胞,PBS轻洗3遍,每孔加入0.5 mL浓度为10μmol/L的DCFH-DA工作液,避光孵育40 min后弃上清液,用无血清培养基洗涤充分后去除多余的DCFH-DA探针,于激发波长488 nm,发射波长525 nm下检测荧光值。
2)SOD酶活力、MDA含量检测。取1.3.4中各组细胞,按照细胞丙二醛(MDA)测定试剂盒、超氧化物歧化酶(SOD)测定试剂盒检测MDA含量、SOD酶活力。
6. 线粒体膜电位检测
取1.3.4中各组细胞,用 PBS溶液清洗1次,加入0.5 mL细胞培养液。随后加入 0.5 mL JC-1 染色工作液,置于37 ℃培养箱中孵育20 min。孵育结束后弃去上清液,用 JC-1 染色缓冲液(1X)洗涤细胞2次。最后,加入1 mL细胞培养液,随即于荧光显微镜下观察并拍照。
7. 对睾酮、双氢睾酮分泌的影响
取1.3.4中各组细胞上清液,以转速3 000 r/min离心20 min,仔细收集上清液于无菌离心管中,睾酮、双氢睾酮分泌水平参照试剂盒说明书进行定量。
8. 数据统计与分析
采用ORIGIN PRO 2021软件对试验数据进行统计分析及作图。多组间比较采用单因素方差分析(One- way ANOVA),以p<0.05表示差异显著。


三、结果与分析
(一)牡蛎肽中氨基酸成分分析
牡蛎肽氨基酸质量分数见表1。
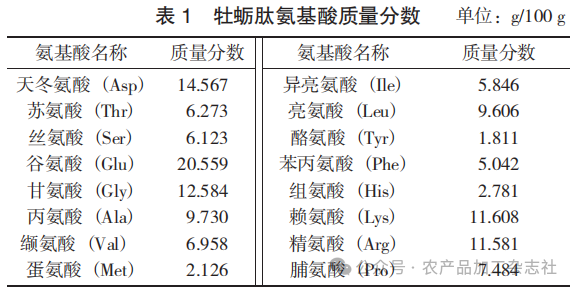
牡蛎肽改善男性性功能的潜力与其独特的游离氨基酸构成密切相关。牡蛎肽所含的人体全部必需氨基酸(包括异亮氨酸、亮氨酸、赖氨酸等),占总游离氨基酸的35.16%,为维持正常的生殖内分泌调控与性腺健康提供了必要的营养基础,研究表明,补充必需氨基酸有助于提升整体新陈代谢及生育能力[8]。而样品中丰富的支链氨基酸(亮氨酸、异亮氨酸与缬氨酸)已被证实能有效增强机体运动能力与缓解疲劳[9],这为保障良好的性功能状态提供了必要的体能支持。此外,牡蛎肽中的精氨酸可通过增强NOS酶活性、促进一氧化氮(NO)生成等在男性勃起生理中至关重要的信号通路,直接维持精子活力[10]。
(二)肽参牡蛎饮对TM3细胞存活率的影响
不同质量分数肽参牡蛎饮对TM3细胞存活率的影响见图1。
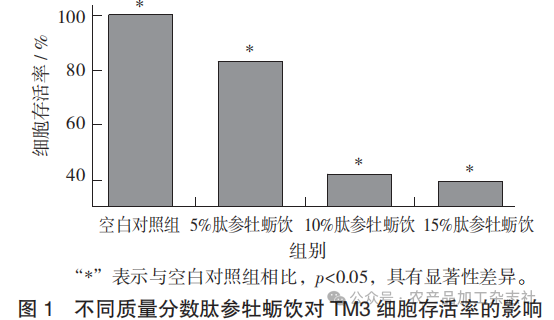
由图1可知,与空白对照组相比,不同质量分数肽参牡蛎饮处理均显著抑制了TM3细胞活力(p< 0.05)。鉴于5%下细胞存活率(83.56%)可保障后续试验的正常生长需求,故被选定为后续加样质量分数。
(三)肽参牡蛎饮对TM3细胞氧化应激水平及线粒体功能的影响
在机体内,过高的活性氧(ROS)水平是诱发氧化应激的关键因素,而生理范围内的氧化状态对维持睾酮正常分泌至关重要[11]。ROS能够攻击生物膜中的多不饱和脂肪酸,引发脂质过氧化反应并生成丙二醛(MDA)。超氧化物歧化酶(SOD)作为体内清除自由基的关键抗氧化酶,在这一过程中发挥核心作用[12]。
肽参牡蛎饮对TM3细胞ROS、SOD酶活力、MDA含量的影响见图2。
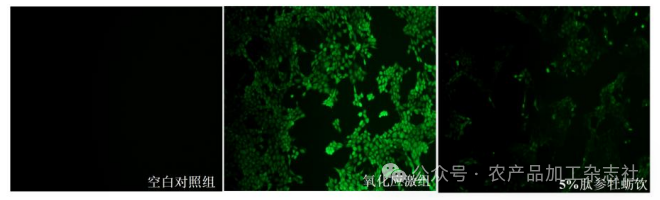
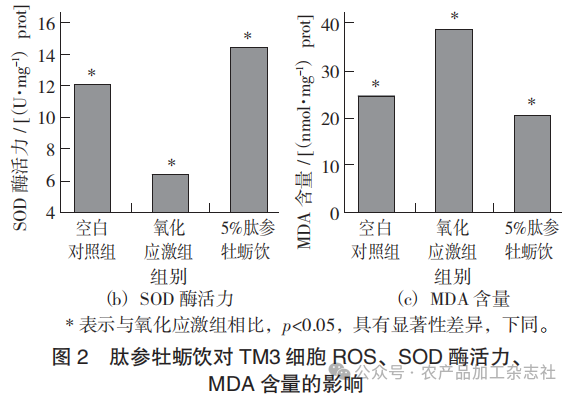
由图2可知,与空白对照组相比,H2O2模型组的TM3细胞中ROS荧光强度与MDA含量显著上升(p<0.05),同时SOD活性显著降低(p<0.05),表明氧化应激模型构建成功。经5%肽参牡蛎饮干预后,细胞内ROS清除率达到58.88%,SOD活性显著提高至14.37 U/mg prot(p<0.05),MDA水平亦显著下降至22.80 nmol/mg prot,表明该处理能有效缓解TM3细胞的氧化应激状态,发挥抗氧化保护作用。持续高ROS导致细胞内氧化还原状态失衡,引起线粒体分子损伤,包括线粒体蛋白和DNA的氧化损伤、膜结构破坏及ATP合成能力下降[13]。
肽参牡蛎饮对细胞线粒体膜电位的影响见图3。
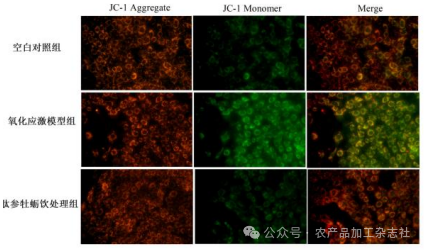
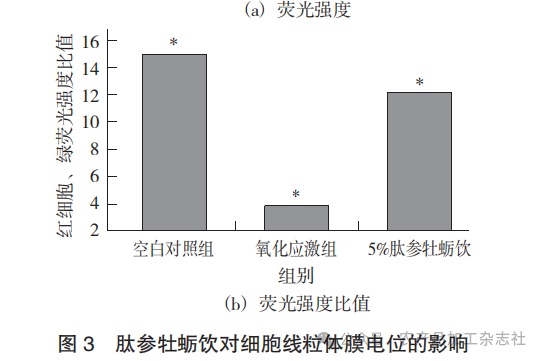
由图3可知,通过JC-1染色检测线粒体损伤,与空白组相比,模型组红/绿荧光比值显著下降(p<0.05),说明线粒体膜电位受损;而经5%肽参牡蛎饮处理48 h后,该比值显著回升(p<0.05),提示线粒体膜电位损伤得到明显改善。线粒体膜电位作为反映线粒体功能的重要敏感指标[14],其损伤与心力衰竭、认知功能障碍及睾丸缺血再灌注损伤等疾病密切相关[15]。综上所述,肽参牡蛎饮可能通过减轻氧化应激、恢复SOD活性、降低MDA含量,并改善线粒体膜电位,发挥对睾丸间质功能的保护作用。
(四)肽参牡蛎饮对睾酮、双氢睾酮分泌结果的影响
为探究肽参牡蛎饮在氧化应激条件下对雄激素合成的影响,检测了TM3细胞中睾酮与双氢睾酮(DHT)的分泌水平。
肽参牡蛎饮对氧化应激状态下睾酮、双氢睾酮分泌的影响见图4。
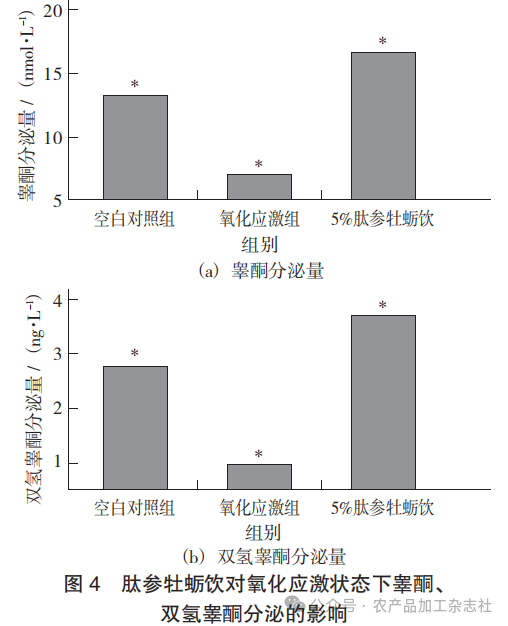
由图4可知,经5%肽参牡蛎饮干预48 h后,细胞分泌的睾酮与DHT含量均较氧化应激组显著升高(p<0.05)。这表明该干预能有效促进睾丸间质细胞合成雄激素。结合前述结果,雄激素水平的恢复可能归因于肽参牡蛎饮有效改善了细胞内的氧化还原状态与线粒体完整性,从而为激素合成创造了有利的生理环境[11]。


四、结论
以氧化应激诱导的功能受损小鼠睾丸间质细胞为模型,探究了肽参牡蛎饮对线粒体功能、睾酮合成及氧化还原平衡的关键调控作用。既证实了“肽参牡蛎饮”在改善男性生殖内分泌功能方面的应用潜力,也为系统深入地评价同类保健饮品提供了可行的研究思路与方法学参考。

编辑:谷金星
审核:关 颖
本篇文章刊登于《农产品加工》2026年2期下