论文推荐 | 基于分子对接技术筛选大菱鲆ACE抑制肽的研究
基于分子对接技术筛选大菱鲆ACE抑制肽的研究
简恒源,赵彦钦,陆佳伟,李燕苹,
张 瑶,张斌成,孔 菲,王晓彤,
代姣南,卢 航,田元勇,鲁雪峰,*赵 慧

作者单位
大连海洋大学
引用格式
简恒源,赵彦钦,陆佳伟,等.基于分子对接技术筛选大菱鲆ACE抑制肽的研究[J].农产品加工,2026,(04):19-24.
基金项目
国家重点研发计划项目(2024YFD2401904);辽宁省教育厅面上项目(JYTMS20230467)。



一、引言
ACE,又称激酶Ⅱ,是一种依赖于锌离子(Zn2+)体现活性,在血压调节中起关键作用的二肽基羧肽酶[1-2]。ACE抑制肽被认为是辅助预防高血压的有效成分,与人工合成肽相比,食源性ACE抑制肽具有无副作用、种类多、易制备等优点[3-4]。2005年,我国首次从鱼蛋白水解物中分离得到高纯度的ACE抑制肽[5]。目前,国际上已报道有上百种海洋生物(如蛤蜊[6]、沙丁鱼[7]、比目鱼[8]等)来源的ACE抑制肽[9]。食源性海洋生物活性肽是预防和治疗生活习惯病更为健康、自然的替代选择[10-11]。
食源性活性肽的提取方法有水解法、酶解法、微生物发酵法、超声波辅助提取法和微波辅助提取法等[12],其中酶解法是目前最为常用的方法之一。通过酶解法制备的多肽能够高效选择性地切断特定肽键,获得较高纯度的目标肽段,且酶解过程不会破坏其生物活性的核心结构[13],酶解产物具有更强的活性。但酶解过程耗时长、成本高是亟待解决的关键问题。计算机模拟技术在虚拟酶解和分子对接方面的应用,为活性肽的研发开拓了新方向[14]。虚拟酶解技术可缩短活性肽纯化过程所需时间,有选择性地筛选所需肽段,进而对肽段进行活性预测和排序[15]。分子对接技术可预测和解析分子之间的相互作用,打分函数软件可预测分子间结合模式和结合强度[16]。因此,计算机模拟技术的应用对活性成分的设计和筛选具有重要的应用价值。
大菱鲆,又称多宝鱼,其肉质鲜嫩、营养价值高[17]。我国大菱鲆产业规模居全球鲆鲽类养殖产业之首[18],是海水鱼类的支柱产业之一,其蛋白含量丰富,鱼蛋白水解产物(FPHs)均有较高的消化率[19],具有较高的开发利用价值。以大菱鲆肌肉蛋白为研究对象,通过计算机虚拟筛选的方法获得具有潜在ACE抑制活性的肽序列,利用分子对接技术阐明潜在活性肽序列与ACE的相互作用关系,进而筛选出具有高结合度的大菱鲆ACE抑制肽,并对筛选出的活性肽进行了体内试验验证,为大菱鲆的深度开发和应用提供理论依据。

二、材料与方法
(一)试验材料
大菱鲆肌球蛋白(Myosin heavy chain 11),通过UniProt蛋白质数据库查询得到[20],从Pdb蛋白质数据库(http://www.rcsb.org)获得ACE的天然晶体结构[21](PDB代码:1O8A)。
ACE天然晶体结构见图1。
(二)试验方法
1. 虚拟酶解和分子对接
以大菱鲆肌球蛋白A0A8D3A461序列为对象,通过BIOPEP-UWM的“Enzyme action”模块在碱性蛋白酶[22](Subtilisin,EC 3.4.21.62)最适条件(pH值8~10,温度25 ℃)下进行虚拟酶解,筛选所得肽段与BIOPEP-UWM[23]和AHTPDB[24]数据库比对获得抗ACE活性肽,并利用Peptide Ranker(活性评分≥0.5)预测高活性肽[25];通过Innovagen分析亲水指数(< 0.5为良好水溶性)[26]、ToxinPred评估毒性(Non- Toxin为无毒标准)[27],结合Expasy-compute预测肽的分子量及等电点[28];基于Discovery Studio 2019对ACE晶体(PDB)预处理(删除杂原子,补全氢原子,定义Zn2+活性中心坐标X:38.997,Y:38.645,Z:50.183,对接半径10Å),构建高活性肽三维结构(Macromolecules模块优化构象),采用半柔性分子对接(CDOCKER模块,受体ACE刚性、配体柔性),以“-CDOCKER Interaction Energy”为量化评估指标[29]进行半柔性分子对接。对接中心设置为(38.997, 38.645,50.183),半径为10Å。
2. 内活性试验验证
1)肽的合成。利用FMOC固相化学合成法分别合成得到肽段RW和RF,肽的纯度均大于90%。
2)试验动物及分组。大鼠置于相对湿度 40%~70%,温度(22±2)℃的 12/12 h 光暗循环的动物饲养室中,自由进食标准鼠粮及饮水。试验采用健康雄性20周龄SHR(自发性高血压大鼠)15只,随机分成3组:空白对照(生理盐水);灌喂组:RW 3 mg/kg、RF 10 mg/kg,经口灌胃后检测0,2,4,6 h的SHR尾动脉收缩压变化情况。所有结果都用平均值±标准误差表示,用变异数分析(One way analysis of va- riance,One way ANOVA)来评估各组之间的差异,p<0.05 为统计显著性水平。试验操作和动物管理均符合大连海洋大学动物伦理委员会的规定,并严格遵循国际试验动物护理与使用指南。


三、结果与分析
(一)计算机虚拟酶解及活性肽的初步筛选
A0A8D3A461经“Enzyme action”在碱性蛋白酶的条件下(pH值8~10,温度25 ℃)虚拟酶解后,共产生了487条肽链,其中具有活性的肽序列有78条,具有ACE抑制活性的肽共有33条、21种,包含12条重复序列。研究中虚拟酶解产生的肽段C端具有多样性,ACE抑制活性的氨基酸多为F、W,且具有较多的水解位点,推测以F、W为C末端肽段具有潜在的ACE抑制活性。
碱性蛋白酶虚拟酶解结果见表1。
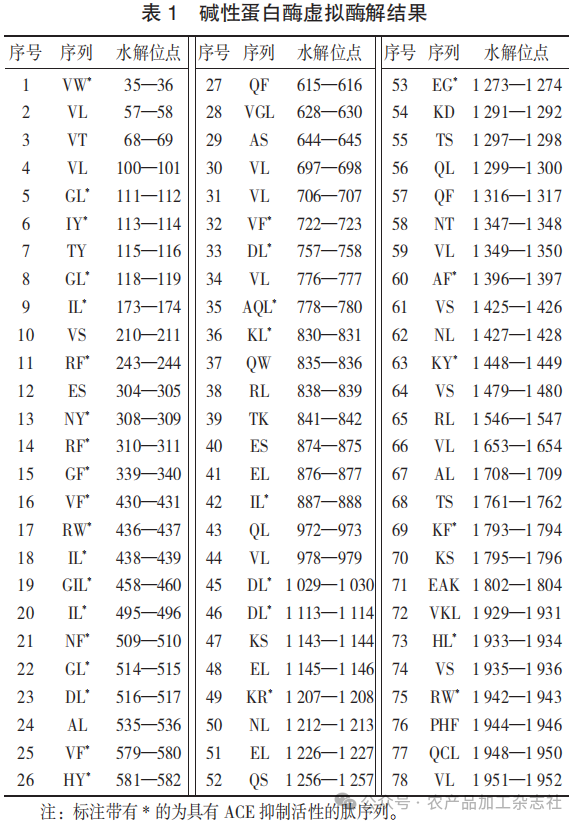
去除重复序列后,通过在线软件Peptide Ran- ker,对生物活性预测后按照活性评分进行排序,统计每种肽的切割位点和分子量。
虚拟酶解的ACE抑制肽活性评分见表2。
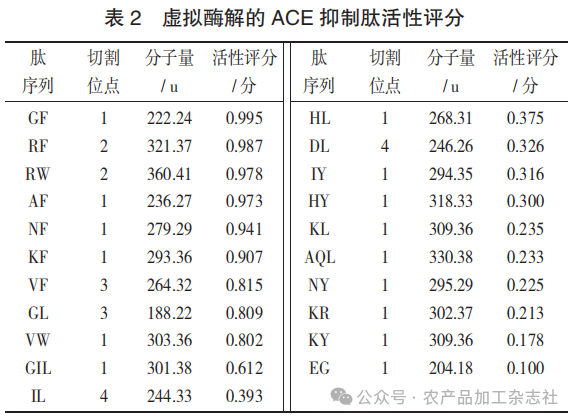
由表2可知,筛选出具有ACE抑制高活性(活性评分> 0.5)的肽共10种,其氨基酸个数为2~3个,分子量为188.22~360.41 u,且净电荷为0~1,碱性蛋白酶特异切断F、L、W链接肽段的C末端,多以F和W为肽链的末端。其中,RF、RW、VF、GL肽段均有多个切割位点,高活性占比高,产生的 ACE 抑制肽活性较强[30],且带有疏水性氨基酸,符合ACE抑制肽的特点。文献中关于WIR序列的研究表明该肽具有较强的ACE抑制活性,这与试验筛选出的序列具有相似结构特征[31]。综上,推测表1中筛选出的10条肽段中实际具有高活性ACE抑制肽的可能性较大,可对其构效关系进行探讨,深入解析肽与ACE的相互作用机制。由此,选择合适的蛋白酶在适当酶解条件下通过计算机虚拟设计高活性海洋来源活性肽是可行的。
(二)毒性预测
通过ToxinPred工具对筛选出的10种高活性且具有ACE抑制活性的肽段进行毒性预测,筛选无毒的活性肽,以避免对人体产生毒害作用[32]。检测的10种肽毒性预测值均为Non-Toxin,可确认为无毒片段。目前,已从多种海洋生物中提取出具有抗ACE活性的肽段,在对北太平洋鱿鱼肌球蛋白肽[33]和马氏珍珠贝肉蛋白[34]的研究中,发现提取的肽无毒性、无致敏性,且具有显著的ACE抑制活性。因此,海洋来源生物活性肽具备安全性,是良好的天然活性肽来源,可作为潜在的食源性ACE抑制活性成分进行应用。
(三)水溶性活性肽的筛选
活性肽的水溶性见表3。
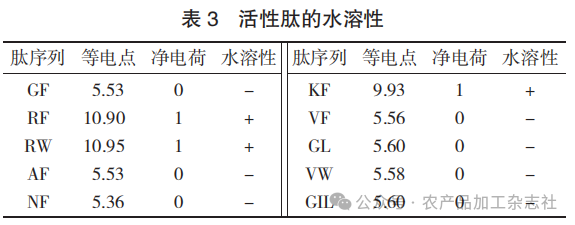
ACE抑制活性与肽段疏水性存在显著相关性[35],ACE抑制率随着肽段疏水性的升高而升高。由表2、表3可知,RF,RW,KF分子量最大为360 u,水溶性良好,易于肠道消化吸收,且均带正电荷,具有潜在的ACE抑制活性。通过分析 10 种活性肽的氨基酸序列,发现多数肽段的氨基酸序列中含有一些疏水性氨基酸,如F、V、L,说明上述肽段具有构成ACE抑制肽的前提基础[36]。
(四)半柔性分子对接
通过Dock Ligands(CDOCKER)模块对筛选出的10条肽段进行分子对接,- CDOCKER 结合能分值(下称为分值)是受体与配体相互作用力的评分,分值越高,表示其结合越紧密[37]。以分值大小评价受体与配体在不同构象下的结合程度,并进行排序,10条待评价肽段中9条分子对接成功,表明具有潜在的ACE抑制活性。
分子对接结果见表4。
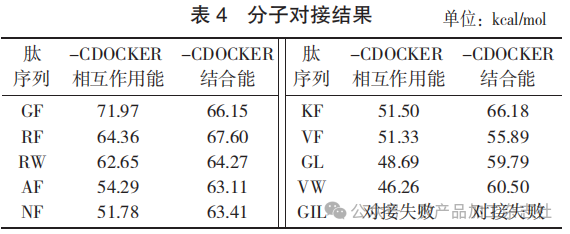
由表4可知,筛选出的高活性肽(活性评分> 0.5)分值为46.259 7~71.967 7。水溶性肽段RW、RF、KF均具有较高分值,这与2.3中活性筛选结果一致,且与已报道的从香豆素中提取的ACE抑制肽活性评分相近[38],说明和ACE分子具有较强的结合力,因此推测可能具有较强的ACE抑制活性。GU Y C等人[39]通过构效分析关系(QSAR)模型从大豆蛋白中分离ACE抑制肽(IC50=53.6 μmol/L),发现IVF,LNF具有较强ACE抑制活性。酪蛋白中的 PERF(IC50= 37.08 μmol/L)[40]及牡蛎蛋白中的VVYPWTTQRF(IC50= 66 μmol/L)[41]均对ACE分子具有非竞争性抑制作用。上述肽段末端分别具有RF,VF及NF片段,研究表明,部分具有相同氨基酸序列的肽可能会具有相似的生物活性[42],结合筛选结果,上述肽段也可能是研究肽段的前体肽,而GIL未能与ACE分子对接,且分子量相对较大,难溶于水,与其他9条肽段相比可能不具备较强活性。综上,含有RW,RF,KF的肽段具有潜在ACE抑制活性。
(五)半柔性分子对接与活性验证
通常,对接分值不能作为评定ACE抑制活性的唯一标准[43],为进一步阐明分子间的作用机制,对分子对接分值高的3条水溶性多肽(KF,RF,RW)与ACE分子的相互作用和结合模式进行分析。
KF的对接构象图见图2,RF的对接构象图见图3,RW的对接构象图见图4。
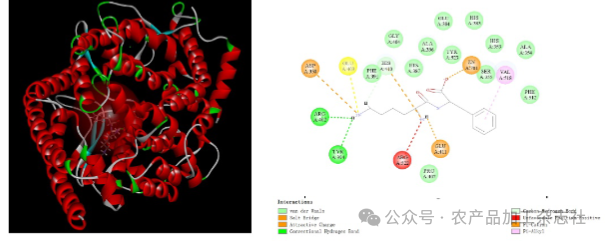

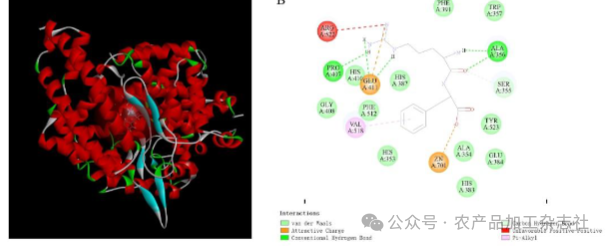

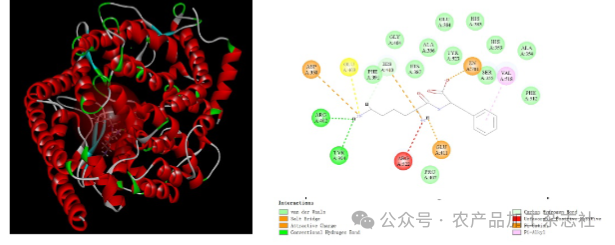

ACE活性部位主要由3个活性口袋组成[44],即S1(Ala354,Glu384和Tyr523)、S2(Gln281,His353, His513,Lys511和Tyr520)和S2'(Glu162),研究表明,与活性口袋S1和S2的氨基酸形成氢键对于维持肽-酶复合物稳定性极其重要[45]。由图3可知,与RW,RF,KF形成氢键的氨基酸残基(Ala354,Glu384和Tyr523)均属于S1口袋,与RW,RF形成氢键的氨基酸残基中有一部分(His353)属于S2口袋,说明 RW,RF能与S2口袋形成紧密的结合,因此RW,RF对接评分略高于KF。YU Z P等人[46]将降血压药物赖诺普利与 ACE 进行分子对接,结果表明,与赖诺普利形成氢键的氨基酸残基(Ala354和Tyr523)部分属于S1口袋;His353属于S2口袋、这与大菱鲆肌源蛋白虚拟水解得到的水溶性活性肽(RW,RF)进行的分子对接具有相似的结果。说明 RW和RF可能具有与赖诺普利的降血压机制相似竞争性抑制作用。
(六)体内活性试验验证
RW和KF经口灌胃SHR后收缩压的变化见图5。
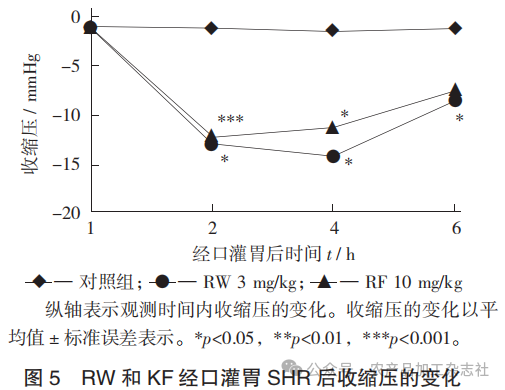
ACE抑制剂的ACE实际抑制活性与分子对接预测结果存在差别[47]。因此,通过分子对接所预测的具有高ACE抑制效果的肽段是否能在生物体内拥有好的降血压效果还需要进一步体内试验来验证。利用Fomc法固相合成RW和RF,经口灌胃SHR后,对其尾动脉收缩压变化进行了探讨。由图5可知,空白组在观测时间内收缩压无明显变化。3 mg/kg的RW和10 mg/kg的RF在经口灌胃后均显著降低了SHR的收缩压,其中RW在4 h后收缩压最低为(-14.00±5.20)mmHg(p<0.05),降血压效果可持续6 h;RF在 2 h后收缩压最低为(-12.00±1.41)mmHg(p<0.001),降血压效果持续4 h。这与草鱼肌肉蛋白肽(GCP)[48]和卵转铁蛋白肽(IRW)的研究结果一致[49]。100 mg/kg剂量的草鱼肽和15 mg/kg剂量的蛋白肽可显著降低SHR的血浆中Angiotensin II水平和ACE活性,从而发挥降血压的效果。而RW和RF均显著降低了SHR的收缩压,且RW和IRW均有RW结构,具有相似的降血压机理,进一步验证了通过抑制ACE活性来达到降血压效果的可能性,RW和RF可能通过抑制ACE活性达到降血压的作用。


四、结论
以大菱鲆肌肉蛋白为研究对象,结合虚拟酶解辅助活性预测和生物信息学方法,进行了初步的活性肽筛选。通过半柔性分子对接方法,将筛选得到的多肽与血管紧张素转化酶(ACE)分子进行对接,探讨了其与ACE分子的结合模式。对接结果表明,RW与ACE中的Ala356,Tyr394,Arg402和His410残基形成了5个氢键;RF则与Ser355,Ala356,Glu411和Pro407残基形成7个氢键;KF与Tyr394,Arg402,His410和Glu411残基形成4个氢键。4种肽分子均通过与ACE中的Zn2+和Val518形成π-π相互作用,显示出与ACE活性中心的显著结合。试验结果表明,肽分子与ACE活性中心的相互作用可能是其具有ACE抑制活性的主要机制。体外试验结果中,RW和RF显示出显著的降血压活性,但其作用机理是否直接与ACE抑制活性相关联仍需进一步研究。综上所述,研究所提出的筛选策略为活性肽的快速筛选提供了一种有效途径,可用于开发新型的ACE抑制剂。同时,也为高血压防治相关活性物质的提取和大菱鲆的高值化利用提供了新思路。

编辑:谷金星
审核:关 颖
本篇文章刊登于《农产品加工》2026年2期下