论文推荐 | 海参肽的酶法制备及其抗氧化活性研究

海参肽的酶法制备及其
抗氧化活性研究
作 者
魏玉萍,张纯霞,
陈梓仪,肖培,*黄永平
作者单位
韩山师范学院生命科学与食品工程学院
引用格式
魏玉萍,蔡琳韩,张纯霞,等.海参肽的酶法制备及其抗氧化活性研究[J].农产品加工,2026,(03):17-21+24.
基金项目
广东省粤东药食资源功能物质与治未病研究重点实验室(2021B1212040015);潮州市科技计划项目( 20190115);韩山师范学院博士教授启动项目(QD20190610),2019年潮州市科技计划项目“海参肽的制备工艺及其关键技术研究”(2019ZC10)
摘 要
海参以高蛋白、低脂肪的特点使其具有抗氧化、抗衰老、抗疲劳等保健功能,对海参肽的酶法制备及其抗氧化活性进行研究。结果表明,木瓜蛋白酶法处理的多肽得率为10.38%,显著高于其他单一酶;而碱性蛋白酶法制备的抗氧化活性最好。通过两两复合酶的比较得出,木瓜蛋白酶与中性蛋白酶复合酶解会产生协同效应,海参多肽得率提升15.51%,其抗氧化活性最高且分别高于木瓜蛋白酶和碱性蛋白酶,复合酶酶解效率优于单一酶酶解效率,为海参肽的提取提供了数据参考。
关 键 词
海参肽;酶解;
抗氧化活性;木瓜蛋白酶;中性蛋白酶
正 文
海参(Sea cucumber,Holothurians)属于棘皮动物门(Echinodermata),海参纲 (Holothuroidea), 是一种重要的海洋无脊椎生物,距今有6亿多年的历史,广泛分布于世界各大海洋中[1]。海参自古以来就被作为重要的营养保健食品,其特点为高蛋白、低脂、低糖、低胆固醇[2]。 然而,海参的利用率只有20%左右。近年来的研究证实,海参蛋白降解为小分子多肽后,吸收率可显著提高达到100%[3]。海参肽是指海参经蛋白酶水解,分离纯化后得到具有特殊生理功能的活性肽[4],不仅具有较好的吸收机制,还具有降血压、抗氧化、促进胶原蛋白分泌、抗疲劳、抗肿瘤等生物活性功能[1,4-5],且来源丰富、安全无毒。目前,国内外对海参肽的研究上较为单一,主要针对于单一酶的提取工艺及抗氧化作用,在研究复合酶提取工艺的方面相对较少。 申彩红[6]研究了6种蛋白酶对海参的酶解工艺并对其进行工艺优化,得出使用中性蛋白酶的最佳酶解条件为酶解温度52 ℃,酶用量6950 U/g,底物质量分数 1.0%,水解时间3h。王静等人[5]研究了海参的酶解工艺和抗氧化活性,结果表明,随着分子量的下降, 海参肽的抗氧化活性逐渐增强。随着科学技术的进步,人们对海参中生物活性物质的药理学作用进行了更进一步的研究,胡越等人[7]采用挤出滚圆法制备了海参肽微丸并进行工艺优化,具有一定的应用价值。 随着人们对海洋资源药用价值关注的日益提高,海参肽在医学与保健领域的应用前景广阔。以刺参为原料,考查单一酶与复合酶的提取工艺及其抗氧化活性,并比较2种酶同步酶解及3种酶同步酶解与单一酶解的差异,优化工艺条件,以期为刺参的高效利用提供数据参考。
1 试验部分
1.1 原料及设备
1.1.1 原料
刺参(加拿大),广州利军达网络科技有限公司提供;碱性蛋白酶、中性蛋白酶、木瓜蛋白酶、海参专用酶(食品级),沧州夏盛酶生物技术有限公司 提供;牛血清白蛋白(标准品),西格玛奥德里奇(上海)贸易有限公司提供;福林酚、2,2 - 联苯基 - 1 - 苦基肼基、七水合硫酸亚铁、酒石酸钾钠、邻苯三酚、无水磷酸氢二钠、无水磷酸二氢钾,均为分析纯,上海麦克林生化科技有限公司提供。
1.1.2 仪器与设备
U/V110Pro 型紫外可见分光光度计,翱艺仪器 (上海)有限公司产品;PTY-B2200 型电子天平,华志(福建)电子科技有限公司产品;QSJ-B03E1型切碎机,小熊电器股份有限公司产品;HH-4型数显 恒温水浴锅,江苏金坛宏华仪器厂产品;TG16-WS型高速台式离心机,湖南湘仪实验室仪器开发有限公司产品;858-1型恒温磁力搅拌器,上海市富成仪器厂产品;FRQ-101型超声波清洗机,深圳福洋科技集团有限公司产品。
1.2 原料预处理
取适量干海参进行3次称量,取平均值并记录,加入去离子水使料液比达到1∶20(g∶mL),置于 15 ℃下充分吸水4d,期间用去离子水换水8次,充分泡发后除去多余水分,进行3次称量,取平均值并记录,计算泡发增质量倍数。将泡发好的海参去除内脏、杂质,用蒸馏水冲洗干净,沥干多余的水分,切成小块,加入10倍量去离子水,用搅拌机打碎、匀浆,保持泡发后海参的质量分数为10%。

1.3 单一酶法制备工艺
取适量海参匀浆液,用浓度为0.05mol/L的HCl 溶液或浓度为0.05 mol/L 的NaOH溶液调节pH值,调至酶的最适值后加酶,按5 000 U/g(相对于泡发 后海参质量)分别添加中性蛋白酶、碱性蛋白酶和木瓜蛋白酶,调节水浴在酶解最适温度范围,搅拌均匀, 酶解 6 h 后升温至 90 ℃,在 90 ℃条件下灭酶 30 min,待酶解液冷却到室温后,以转速 8 000 r/min 离心 10 min,过滤上清液,对可溶性多肽含量、抗氧化活性进行测定。考查不同酶的酶解效率,筛选最适合的海参水解酶。
单一酶解条件见表 1。
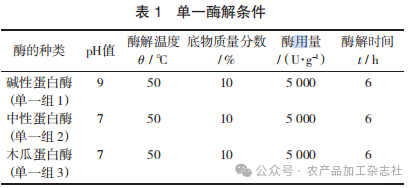
1.4 复合酶法制备工艺
采用碱性蛋白酶、中性蛋白酶和木瓜蛋白酶两两 复合及3种复合,与海参肽专用酶进行对比。适量的海参匀浆液,用浓度为 0.05 mol/L的HCl溶液或浓度为 0.05 mol/L的NaOH溶液调节pH值至7.0,用去离子水稀释至海参质量分数为10%,分别于50 ℃温度下,加入复合酶5 000 U/g,同时酶解 6 h。反应完成后测定可溶性多肽含量、抗氧化活性。
复合酶解条件见表 2。
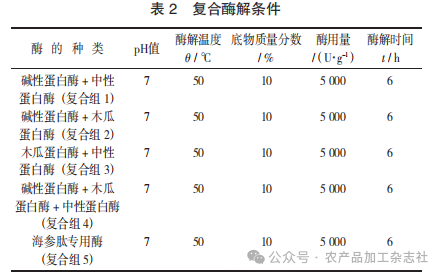
1.5 可溶性多肽含量的测定
参考文献[8]中的福林 - 酚试剂法,测出可溶性多肽含量。由于蛋白质中的肽键与碱性铜盐反应生成深蓝色复合物,复合物颜色的深浅与含量呈正相关,使用分光光度计于波长 640 nm 处测定其吸光度,再根据计算所得的标准曲线对照得到蛋白质含 量,从而确定可溶性蛋白质含量。
1.5.1 牛血清白蛋白(BSA)标准曲线的绘制
精确称取牛血清白蛋白固体 25 mg,溶于 H2O, 定容至 100 mL 得到母液。分别精准配制蛋白质量为0,25,50,100,150,200,250μg的 7 支 1 mL 对照母液于试管内。利用福林酚法测定蛋白质质量浓 度,并绘制蛋白质量浓度(X)与吸光度(Y)的标准 曲线,回归方程为Y=0.0024X+0.0046,R2=0.999 9。
1.5.2 海参蛋白酶解液可溶性多肽质量分数的测定
从提取液中各取水解液 1 μL,稀释 100 倍,随后从稀释液中各移取 1 mL 按照 1.5.1 步骤操作,于波长 640 nm 处测定吸光度,试验重复测定 3 次,结果取平均值。根据绘制的标准曲线计算样品中 BSA 量,按照公式(2)计算,可得到样品中可溶性多肽质量分数[9] 。

1.6 不同海参肽酶解液抗氧化活性的测定
1.6.1 清除 DPPH 自由基能力的测定
参照SHARMA O P 等人[9]的测定方法并稍作调整。试验设定样品组、对照组和参比组。①样品组: 提前将样品溶液配置成不同质量浓度,依次吸取 1 mL 酶解溶液于试管中,加入浓度为 0.1 mmol/L的 DPPH 乙醇溶液 4 mL,涡旋振荡混匀后避光静置 30 min,于波长 517 nm 处测定吸光度(A)。②参比组:以等体积无水乙醇替换 DPPH 乙醇溶液,同样方法测定吸光度(A)0 。③对照组:用等体积超纯水替换海参提取液进行测定的吸光度(A1 )。所有测定设置 3 个 生物学重复,数据取平均值。按照公式(3)计算,可得到不同海参肽酶解液对 DPPH 自由基清除率。

1.6.2 清除羟自由基能力的测定
提前将样品溶液配置成不同质量浓度,依次吸取酶解溶液 1 mL 于试管中, 依次移取浓度为 9 mmol/L 的 FeSO4 溶液和浓度为 9 mmol/L 的水杨酸-乙醇溶液各1 mL于试管内,最后再加入 1 mL 浓度为 8.8 mmol/L 的 H2O2,混匀,在 37 ℃条件下反应 1 h,于波长 510 nm 处测定吸光度[10],用等体积 H2O 代替 H2O2 测 定吸光度(A)2,以等体积 H2O 替换样品浓度测定其吸光度(A)0 。 试验重复测定3次,结果取平均值。按照公式(4)计算,可得到不同海参肽酶解液对羟自由基清除率,以样品质量浓度为横坐标,羟自由基清除率为纵坐标,绘制关系曲线。

1.6.3 清除超氧阴离子能力的测定
提前配置浓度为 0.1 mol/L 的磷酸缓冲液(pH 值 8.04),浓度为 10 mmol/L 的邻苯三酚溶液。移取 1 mL 蒸馏水和上述邻苯三酚溶液到 3.5 mL 的磷酸缓冲液中,计时的同时迅速振荡均匀。0.5 min 后,于波长 325 nm 处测定吸光度(A)1 ,随后以 0.5 min 为间隔持续记录其吸光度变化,直到 3.5 min后记录最终值(A)2 ,据此计算样品存在条件下的自氧化速率(S)1 。空白对照组以等体积 10 mmol/L HCl 溶液替代邻苯三酚溶液,测定体系本底自氧化速率(S)0 。准确测定 1 mL 不同质量浓度的海参寡肽和海参多肽溶液,按上述方法加入样品后测定溶液的吸光度[11] ,每个质量浓度组平行测 3 次后取平均值, 并计算加入样品后邻苯三酚的自氧化率。制作样品质量浓度(X)与超氧阴离子清除率(Y)的关系曲线。

2 结果与分析
2.1 海参原料预处理
根据试验结果得到增质量倍数为4.64±0.17的泡发刺参。
泡发增质量倍数见表3。
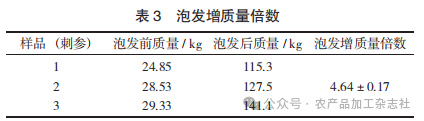
2.2 可溶性多肽含量结果分析
单一酶解液可溶性多肽质量分数见图 1。
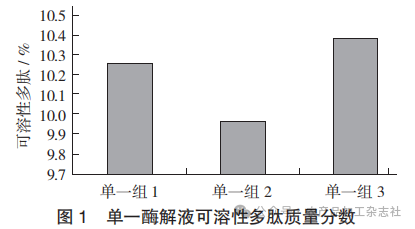
3种酶解液采用福林-酚试剂法测定出其可溶性 多肽质量分数。由图 1 可知,得出 3 种单一酶解液 中有 9.97%~10.34%的可溶性多肽,其中单一组3可溶性多肽质量分数最高(木瓜蛋白酶,10.38%),其次是单一组1(碱性蛋白酶,10.26%)和单一组2(中性蛋白酶,9.97%)。木瓜蛋白酶水解多肽的研究 结果与于淑池等人[12]相似,采用木瓜蛋白酶和碱性蛋白酶对光参酶解,多肽得率与试验结果十分相近。杨 颖等人[13]利用中性蛋白酶水解加拿大红参,多肽得率为 13.99%,略高于试验结果,这可能与原料的不同有关。
复合酶解液可溶性多肽质量分数见图2。
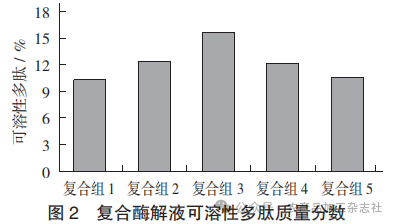
由图2可知,4种复合酶解液与海参专用酶解液 通过福林-酚试剂法测定出可溶性多肽质量分数,得出4种复合酶解液中含有 10.30%-15.51%可溶性多肽, 其中复合组3质量分数最高,为15.51%;其次是复合组2,质量分数为12.38%;再次复合组4,质量分数为 12.05%;复合组1质量分数最低,为 10.30%;且复合组5与复合组1—复合组4进行对比,质量分数仅高于复合组1,为10.34%。与单一酶进行对比,多肽质量分数增高。相似的很多研究 报道了类似结果,王迪等人[14]以枯草杆菌中性蛋白酶 与风味蛋白酶组成复合酶酶解北极参,多肽得率为 15.38%,且复合酶的多肽得率高于木瓜蛋白酶的多肽得率。于淑池等人[12]用复合酶水解光参的多肽得率高于单一木瓜蛋白酶水。不同酶作用后的多肽得率有所差异,酶作用位点不同导致蛋白水解的结果也有所不同,复合酶的使用有助于生成更多具有特定生物活性的小分子肽段,能够进行更加全面的水解,从而释放更多的可溶性多肽[15]。
2.3 不同海参肽酶解液抗氧化活性
2.3.1 清除 DPPH 自由基能力
单一酶解液清除 DPPH 自由基能力见图3。
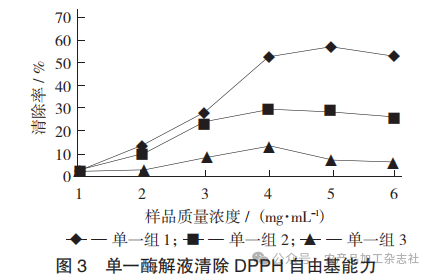
由于 DPPH 自由基很稳定,利用这一特点将 DPPH 自由基代替生物体内的自由基,可弥补生物体内自由基维持时间短的缺点,作为抗氧化活性的指标。3 组样品在质量浓度为 1~4 mg/mL时,随着样品质量浓度的增加,DPPH 自由基清除能力不断增强,其中单一组2 与单一组3均达到最大清除率,分别为29.9%和 13.8%。而单一组1随着样品质量浓度继续升高,DPPH 自由基清除能力继续升高,在样品质量浓度为5 mg/mL 时达到最大清除率,为57.2%。由图3可知,单一组1(碱性蛋白酶)有最好的 DPPH 自由基清除能力,其次是单一组2(中性蛋白酶)。
复合酶解液清除 DPPH 自由基能力见图4。
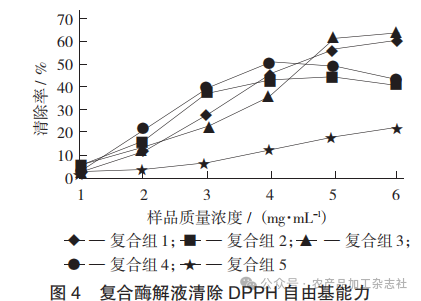
由图4可知,样品质量浓度为 1~4 mg/mL 时,5 种酶解液的 DPPH 自由基清除率随样品质量浓度的增加而增强,复合组4和复合组2有最大的 DPPH 自由基清除率,分别为 50.2%和 43.1%,样品质量浓度继续增加,2种样品的 DPPH 自由基清除力开始下降。而另外3种样品随着质量浓度增加,DPPH 自由基清除能力继续增加,在样品质量浓度为6 mg/mL 时,复合组3和复合组1有最大的自由基清除率,分别为63.7%和60.2%;复合组5的自由基清除率最低。与图3相比,除复合组5之外,其他复合酶解液的 DPPH 自由基清除力均明显升高。
2.3.2 清除羟自由基能力
单一酶解液羟自由基清除能力见图5。
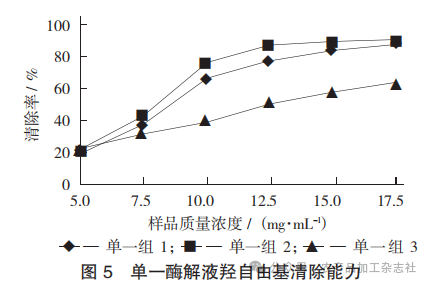
由图5可知,在样品质量浓度为5.0~12.5 mg/mL 时,3种单一酶解液对羟自由基的清除率与海参的质 量浓度呈正相关,随着质量浓度的升高,羟自由基 清除率显著增加,且单一组2与单一组1明显高于单一组3的清除率;在海参质量浓度为12.5~15.0 mg/mL 时,增加较为平缓;样品质量浓度为17.5 mg/mL 时,单一组1(碱性蛋白酶)和单一组2(中性蛋白酶)有最大的羟自由基清除率,为 91.0%。
复合酶解液清除羟自由基能力见图6。
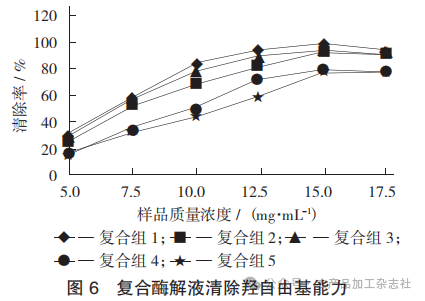
由图6可知,当样品质量浓度为5.0~15.0 mg/mL 时,随着样品质量浓度的增加,5 种复合酶的羟自由基 清除率稳步增高,其中复合组1、复合组2、复合组3的清除率接近100%;而在样品质量浓度为17.5 mg/mL 时,5 种复合酶的羟自由基清除率均有所下降,且海参专用肽酶的羟自由基清除率最低。与图5 相比,复合酶解液的羟自由基清除能力明显升高。
2.3.3 清除超氧阴离子能力
单一酶解液清除超氧阴离子能力见图7。
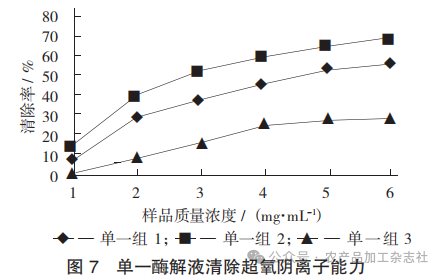
由图7可知,随着样品质量浓度的增加,清除超氧阴离子能力也随之增强。3种酶解液对清除超氧阴离子能力依次为单一组 2 > 单一组 1 > 单一组 3。碱性蛋白酶的抗氧化活性最好,与梁杰等人[16]用碱性蛋白酶酶解海参肽有较好的抗氧化活性相符。
复合酶解液清除超氧阴离子能力见图8。
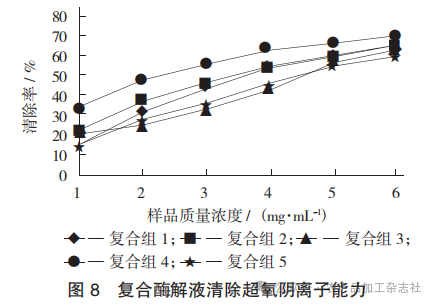
由图8可知,酶解液对超氧阴离子的清除能力随着样品质量浓度的增加而增强。当样品质量浓度为6 mg/mL时,清除超氧阴离子能力增长速率有所降低, 且复合组4的清除率最高为69.4%,复合组5的清除率最低为59.8%。碱性蛋白酶与中性蛋白酶复合酶解高于碱性蛋白酶酶解的抗氧化活性,说明在不同酶解液的抗氧化活性研究上,复合酶比单一酶活性好;两两复合酶解的抗氧化活性优于3种酶酶解的抗氧化活性,可能是由于不同酶的酶解条件不同,3种酶取适宜的中间酶解条件进行同步酶解所导致的抗氧化活性降低。
3 结论
对复合酶与单一酶酶解海参的酶解液多肽含量进行了比较,复合酶解中采用2种酶酶解及3种酶酶解进行研究。结果表明,采用木瓜蛋白酶与中性蛋白酶的复合酶解液可溶性蛋白质量分数最高,为 15.51%。对酶解液抗氧化活性进行研究发现,复合酶的抗氧化活性高于单一酶及3种酶的抗氧化活性。 试验结果为充分利用海参资源,开发具有抗氧化功效的功能食品提供了理论依据。
参考文献:
[1]SROYRAYA M,HANNA P J,SIANGCHAM T,et al. Nutritional components of the sea cucumber olothuria scab - ra [J] . Functional Foods in Health and Disease2017(3):168-181.
[2]杜美玲,陈忻,欧阳永中,等. 海参营养成分及加工技 术的研究进展[D] . 佛山:佛山科学技术学院, 2020.
[3]马震雷,郑萍. 海参多肽提取工艺研究[J] . 安徽农业科学,2012,40 (34):16815-16817.
[4]倪明龙,黄海潮. 海参肽的生物活性及其应用研究进展[J] . 轻工科技,2020,36 (8):16-17,20.
[5]王静. 海参多肽的酶法制备及体外的抗氧化活性研究[D] . 烟台:烟台大学,2010.
[6]申彩红. 海参肽的酶法制备及其抗氧化、抗疲劳活性研究[D] . 泉州:华侨大学,2015.
[7]胡越,缪怡烨,喻樊,等. 海参多肽微丸制备工艺[J] . 食品工业,2021,42 (6):138-142.
[8]杨坤. 7 种海参提取物酶法制备及其抗氧化活性研究[J] . 中国食品学报,2019,19 (9):128-136.
[9]SHARMA O P,BHAT T K. DPPH antioxidant assay revisited [J] . Food Chemistry,2009 (4):1202-1205.
[10]苏晓雨,王振宇. 红松子种皮提取物活性成分及抗氧化作用研究 [J] . 林产学工业,2010,30 (1):99-102.
[11]尹大芳. 海带中多种单糖组成检测技术及海带多糖纯化、酶解研究 [J] . 上海:上海海洋大学,2021.
[12]于淑池,张鸣芯. 光参多肽的酶解制备工艺及其功能特性研究 [J] . 中国食品添加剂,2021 (5):60-67.
[13]杨颖,汪秋宽,谷越,等. 加拿大红参(Parastichopus californicus)基本成分分析及其酶解工艺研究[J] . 食品工业科技,2016,37 (1):190-194,200.
[14]王迪,宋悦凡,刘舒,等. 北极参多肽酶解工艺优化[J] . 河北渔业,2017 (5):38-43.
[15]张健,刘少伟,张毅,等. 仿刺参精低分子质量多肽的制备及抗氧化作用 [J] . 食品科学,2016,37 (12):248-253.
[16]梁杰,汪少芸. 海参蛋白肽工艺制备优化及抗氧化性质[J] . 莆田学院学报,2016,23 (2):67-71.◇
编辑:谷金星
审核:关 颖
本篇文章刊登于《农产品加工》2026年2期上