基于抗氧化活性的绿茶功能性成分提取及品质研究
论文推荐 | 基于抗氧化活性的绿茶功能性成分提取及品质研究

基于抗氧化活性的绿茶功能性成分提取及品质研究
作 者
韩梦霞,李阿慧,张煜钦,梁欣怡,
*索茂荣,鄢圣英,董晓勤
作者单位
浙江农林大学 暨阳学院
引用格式
韩梦霞,李阿慧,张煜钦.基于抗氧化活性的绿茶功能性成分提取及品质研究[J].农产品加工,2026,(03):9-16.
基金项目
浙江农林大学暨阳学院大学生科技创新活动计划项目 (JYKC2378)
摘 要
采用热水浸泡法制备绿茶提取物,以抗氧化活性为筛选指标,通过正交试验法优选绿茶提取工艺; 采用 DPPH 自由基和羟自由基的清除率评价绿茶的抗氧化能力,比色法检测绿茶多酚、黄酮、多糖的质量分数,典型相关法分析绿茶抗氧化活性与多糖、黄酮、多酚成分之间的相关性,聚类分析法对不同品种绿茶进行相似性分析。结果表明,绿茶水提物的最佳提取条件为浸泡温度90 ℃,浸泡时间 25 min,料液比1∶30(g∶mL);DPPH 自由基清除力和羟自由基清除力最强的绿茶分别是湖南的武当绿茶和广西的清明毛尖,半数抑制有效质量浓度分别为4.29 mg/mL 和6.57 mg/mL,抗氧化活性成分主要是多酚。不同产地不同品种绿茶在抗氧化能力、化学成分、浸出物等方面具有差异性。绿茶抗氧化物质的提取工艺简单, 适合工业化大生产。
关 键 词
绿茶;抗氧化作用;
提取工艺;正交试验;多酚
正 文
绿茶含有丰富的营养功能物质,如茶多酚、黄 酮、茶多糖、茶氨酸、咖啡碱、氨基酸、维生素等。由于其特殊风味及抗氧化、延缓衰老的特性,绿 茶逐渐取代红茶成为我国饮用最为广泛的一类茶[1]。我国是世界第一大茶叶生产国,茶叶资源十分丰富,绿茶产区分布广,其中浙江、湖北、四川、云南、安徽、江苏、山东等地为主要的绿茶种植区。不同产区绿茶由于品种、地理环境和气候等差异,其含有的化学成分和生物活性也存在很大差异[2-3]。因此,探究不同产地不同品种绿茶的抗氧化能力,对促进绿茶保健养生、提升绿茶品种选育和产业化发展具有重要意义。绿茶的特色功能成分主要是茶多酚、黄酮和多 糖,其中茶多酚具有多种生理活性,如调节肠道菌 群[4-5]、提高免疫力[6]、保肝[7]、抗炎[8]、抗病毒[9]、抗癌[10]、降血脂[11]、保护血管[12]、抗氧化[13]等。因此,茶多酚被广泛应用在医疗保健和功能食品中。绿茶含有丰富的黄酮类物质,如儿茶素、 芦丁、茶黄素等,黄酮类物质具有抗癌[14]、降血脂[15]、 保肝[16]、 抗氧化[17]、 延缓衰老[18] 等功效,这也是饮茶具有保健养生的原因之一。绿茶中的多糖亦具有多种生理活性,如抗氧化[19]、免疫调节[20]、降血糖[21]、降血脂[22]、抗癌[23]等,也是茶叶中极具开发价值的一类生理活性物质,在医药和食品领域有广阔的应用前景[24]。西湖龙井是中国绿茶的代表性品种,以西湖龙井为原料,基于养生保健的实际需求,研究不同冲泡条件,如浸泡时间、水温、 加水量对绿茶抗氧化 活性的影响,通过单因素试验和正交试验优化绿茶 的冲泡工艺。以优化条件研究 10 种不同地区不同绿茶的抗氧化活性,比较不同产地不同品种绿茶在保 健养生方面的品质差异。为阐明绿茶的抗氧化能力及最佳提取条件,以抗氧化活性为筛选指标,对绿茶抗氧化活性物质的提取工艺进行优化,通过DPPH自由基和羟自由基的清除率评价绿茶抗氧化能力,分析抗氧化活性与多糖、黄酮、多酚之间的相关性,以优选条件对10 种不同产地不同品种绿茶进行抗氧化作用和活性成分分析,以期为抗氧化养生保健绿茶的选择提供依据。
1 材料与方法
1.1 材料与试剂
绿茶产地信息见表 1。
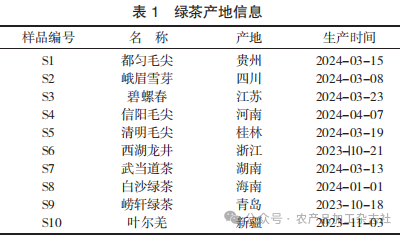
福林酚、芦丁、葡萄糖、没食子酸,浙江常青化工有限公司提供;DPPH试剂,福建领江生物科技有限公司提供;硫酸亚铁、双氧水、无水乙醇、亚硝酸钠、水杨酸、硝酸铝、30%过氧化氢,上海广诺化学科技有限公司提供。
10 种绿茶外观特征见图 1。
图1 10种绿茶外观特征
1.2 仪器与设备
BPG-9040A 型恒温鼓风干燥箱,上海一恒科学 仪器有限公司产品;HH-501型超级恒温水浴锅,常 州国华电器有限公司产品;旋转蒸发仪,艾卡(广 州)仪器设备有限公司产品;UV-2600 型紫外可见 分光光度计,岛津仪器(苏州)有限公司产品; SHB- Ⅲ型循环水式多用真空泵,郑州长城科工贸有限公司产品; ReadMax1900 型光吸收全波长酶标仪,上海闪谱生物科技有限公司产品;FC5816R 型高速冷冻离心机,奥豪斯公司产品。
1.3 试验方法
1.3.1 绿茶浸出液的制备
精密称取2 g 新鲜绿茶,按照实验设计加一定比例不同温度的蒸馏水,浸泡一定时间,过滤,滤液以5 000 r·min-1 离心15 min,取上清液,定容到50ml容量瓶,得绿茶浸出液。取其中10毫升,进行冷冻干燥,得绿茶浸出物。
1.3.2 绿茶粗多糖制备
将绿茶提取液浓缩至含原料浓度为 0.5g/mL的浓缩液,加两倍体积的85%乙醇,4 ℃ 低温静置12h,过滤,将沉淀物干燥,得绿茶粗多糖。
1.3.3 绿茶对DPPH自由基清除力测定
参考邵郅胜[25]的方法。用70%乙醇配制浓度为1、2、4、8、16 mg/mL的样品溶液,取3 mL于具塞试管中,加3 mL 0.2 mmol/L DPPH溶液,摇匀,25℃下避光反应30 min,测定反应液在517 nm处吸光值A。
1.3.4 绿茶对羟自由基的清除能力
参考文献[25]的方法。配制质量浓度分别为1、2、4、8、16mg/mL的绿茶提取液,依次加入9 mmol/L FeSO4溶液、9 mmol/L邻羟基苯甲酸-乙醇溶液各1 mL、8.8 mmol/L H2O2溶液各10 mL,混匀,保持37℃反应15 min,测定样品溶液在510 nm处的吸光度值记为A。 1.3.5 绿茶粗多糖质量分数测定
1.3.5 绿茶粗多糖质量分数测定
采用苯酚-硫酸比色法检测多糖[26]。标准曲线的绘制,取干燥葡萄糖标准品50.0 mg,加水配制成浓度为0.1 mg/mL的葡萄糖标准液。精密量取标准液0.2、0.4、0.6、0.8、1.0 m L,置于10 mL容量瓶,加2mL蒸馏水,5%苯酚溶液1.0 mL,浓硫酸5.0 mL,加蒸馏水定容, 40 ℃ 水浴中保温 15 min,混合反应液于490 nm处测定吸收度,以吸光度(y)为纵坐标,浓度(x)为横坐标绘制标准曲线,得线性回归方程: y = 0.0124x + 0.115,r=0.9944。绿茶粗多糖的含量测定方法同“标准曲线的绘制”,根据线性回归方程,计算多糖含量(mg/g)。
1.3.6 黄酮含量的测定
采用硝酸钠-硝酸铝-氢氧化钠比色法测定黄酮含量[27]。精密称取25mg芦丁标准品,置于25mL容量瓶,加95%乙醇溶解并定容,得1mg/mL芦丁标准品溶液;精密量取0.5、1、2、2.5、3mL芦丁标准品溶液,分别置于25mL容量瓶中,各加水6mL,5%亚硝酸钠溶液2.5mL,摇匀,静置6min,加10%硝酸铝溶液1.5mL,摇匀,静置6min,加5%氢氧化钠溶液7.5mL,加95%乙醇至刻度,摇匀,静置15min,以不加标准品的对照管为空白对照,在510nm波长处测定吸光度。以芦丁标准品的质量浓度(x)为横坐标,以吸光度(y)为纵坐标,得线性回归方程:y = 0.0831x + 0.0815,r=0.9981。精密吸取0.2mL绿茶浸出液,测定操作同“标准曲线的绘制”,根据线性回归方程,计算黄酮含量(mg/g)。
1.3.7 多酚含量测定
采用福林酚比色法测定多酚含量[28]。准确称取没食子酸标准品,配制成质量浓度分别为0.015、0.075、0.15、0.225、0.3、0.375mg·mL-1的没食子酸标准液。吸取上述标准品溶液各1mL,加入50毫升容量瓶,依次加入20mL双蒸水和 3mL福林酚工作液,室温下避光静置5min,加12 mL 10%NaCO3溶液,混匀后加蒸馏水定容,于30℃水浴锅中避光反应2h,在765nm波长处测定吸光度值。以没食子酸浓度(x)为横坐标,吸光度值(y)为纵坐标作图,得线性回归方程:y=0.0366x+0.1006,r=0.9831。绿茶样品溶液的测定同“标准曲线的绘制”。根据线性回归方程,计算多酚含量(mg/g)。
1.3.8 单因素试验
按照1.3.1制备方法,在其他条件相同的情况下,以绿茶对DPPH和羟自由基的清除能力为考核指标,考察浸泡温度(60℃、70℃、80℃、90℃、100℃)、浸泡时间(5min、10min、20min、30min、50min)、固液比(1:10、1:20、1:30、1:40、1:50 g/mL)对绿茶抗氧化活性的影响,确定各因素优水平。研究某一因素时,其他因素的控制变量分别是料液比1:30,浸泡时间20min,浸泡温度80℃。
1.3.9 正交试验
在单因素试验结果基础上,正交试验法优化绿茶的提取工艺,单因素试验结果提示绿茶清除DPPH的作用强于对羟自由基的作用,因此,以绿茶对DPPH自由基的清除率为指标,以浸泡温度(A)、浸泡时间(B)、固液比(C)作为考察因素,设计三因素三水平正交试验。
正交试验因素与水平见表 2。

1.3.10 数据处理
采用SPSS 26.0版软件进行均值统计、相关性、聚类分析,组间统计差异采用单因素方差分析(ANOVA)分析。折线图、柱状图和相关性热图均用GraphPad Prism 9.0软件绘制。
2 结果与分析
2.1 浸泡温度对绿茶抗氧化能力及活性成分的影响
浸泡温度对绿茶抗氧化能力和活性成分质量分数的影响见图 2。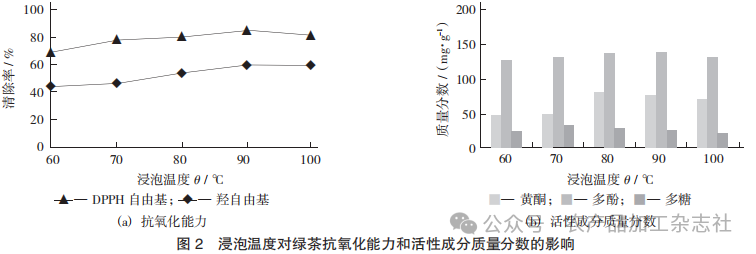
在料液比1:30,提取时间20min 的条件下,考察水温(60℃、70℃、80℃、90℃、100℃) 对绿茶清除DPPH自由基和羟自由基能力的影响。如图2(a), 温度不同,绿茶的抗氧化作用不同,在本试验所设温度范围内,随着浸泡温度增加,绿茶浸出物(6 mg/mL,以绿茶原料计算)对DPPH和羟自由基清除率都呈现先增加后缓慢降低的趋势,在90℃时所得绿茶提取物清除DPPH和羟自由基能力最强。相同条件下,绿茶对DPPH的清除作用大于对羟自由基的作用。
活性物质含量检测结果如图2(b),随着温度升高,绿茶中的黄酮、多酚、多糖呈现先增加后下降的趋势,90℃条件下绿茶浸出物多酚含量最高,80℃条件下绿茶浸出物黄酮含量最高,70℃条件下绿茶浸出物多糖含量最高,说明绿茶的抗氧化性与黄酮和多糖的含量没有剂量依赖性。基于绿茶的抗氧化保健效果,该研究结果亦说明绿茶不适合开水泡,建议90℃左右的热水冲泡。
2.2 浸泡时间对绿茶抗氧化能力及对活性成分的影响
浸泡时间对绿茶抗氧化能力和活性成分质量分数的影响见图3。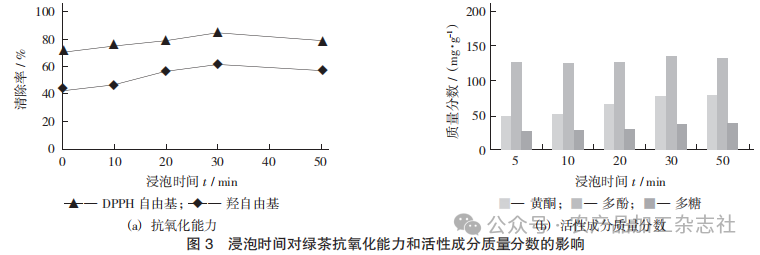
由图3(a)可知,随着浸泡时间延长,绿茶浸出物(6 mg/mL)对 DPPH 自由基和羟自由基的清除作用呈现先增强后减弱的过程,浸泡时间为 30 min 所得绿茶提取物抗氧化作用最强;相同条件下,绿茶对 DPPH 自由基的清除作用大于对羟自由基的清除作用。由图3(b)可知,随着浸泡时间延长,多酚、黄酮、多糖逐渐浸出,其中多酚呈现先增加后下降的趋势,在 30 min 时,多酚质量分数达到最大。多糖和黄酮在试验所设浸泡时间范围内,质量分数一直在升高,但抗氧化性没有同步增加,推测多糖可能不是绿茶清除 DPPH 自由基和羟自由基的主要成分,表明不同浸泡时间下,绿茶提取物的抗氧化活 性与黄酮和多糖的质量分数无剂量依赖性。
2.3 料液比对绿茶抗氧化能力及对活性成分的影响
料液比对绿茶抗氧化能力和活性成分质量分数的影响见图4。
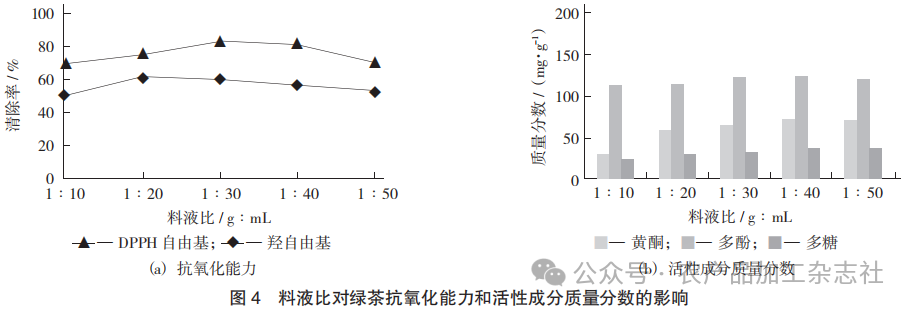
由图4(a)可知,料液比不同,绿茶的抗氧化 作用不同。随着溶剂量增加,绿茶抗氧化活性呈现 先增加后降低趋势,相同条件下,绿茶对 DPPH 自 由基的清除作用大于对羟自由基的清除作用。在料 液比为 1∶30 时,绿茶清除 DPPH 自由基能力达到 最大;在料液比为 1∶20 时,绿茶清除羟自由基能 力最大。
由图4(b)可知,随着料液比的增加,绿茶黄 酮、多酚、多糖的质量分数呈现先上升后下降的趋 势,当料液比为 1∶30 时,多酚质量分数最高;当 料液比为 1∶40 时,黄酮和多糖的质量分数最高。 绿茶清除羟自由基能力与这3类成分的质量分数无剂量依赖性,说明绿茶可能含有其他清除羟自由基的活性成分。
2.4 正交试验结果
正交试验设计与结果见表3,正交试验方差分析见表4。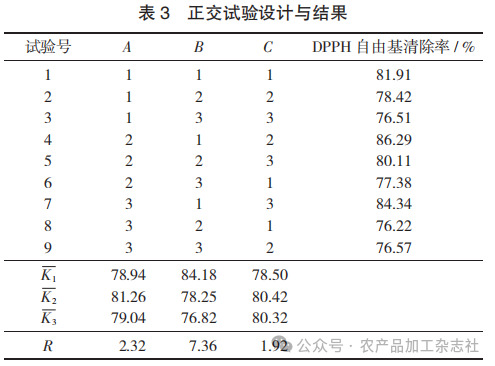
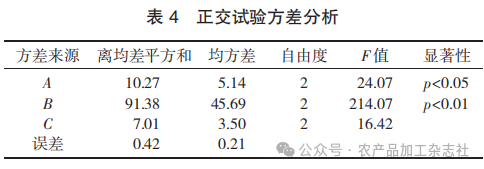
由表3和表4可知,3个因素的主次顺序为B> A>C,即浸泡时间 > 浸泡温度 > 料液比,其中浸泡 温度(p<0.05)和浸泡时间(p<0.01)对绿茶的抗 氧化效果具有显著影响。根据正交试验结果及方差 分析可得出最佳因素水平组合为 A2B1C2,即浸泡温 度 90 ℃,浸泡时间 25 min,料液比 1∶30,所得绿茶提取物清除 DPPH 自由基能力最强,为最佳浸泡 条件。
2.5 绿茶对DPPH自由基的清除作用和聚类分析
不同品种绿茶清除DPPH自由基能力和聚类分析见图5。
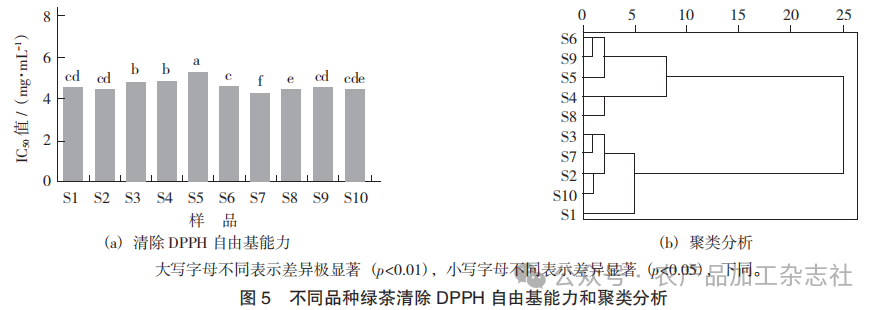
以优选提取条件对10种绿茶进行提取,对所得绿茶提取物进行抗氧化作用与活性成分质量分数分析。 不同品种绿茶对DPPH自由基的清除作用不同,10 种绿茶对DPPH自由基的半数抑制有效质量浓度为 4.29~5.51 mg/mL,其中 S7 对 DPPH 自由基的清除作用最大,并与其他品种绿茶具有显著性差异。以绿茶对 DPPH 自由基的 IC50 为变量,对绿茶进行系统聚类分析。由图 5(b)可知,当欧式距离平方和为10 时,10 种绿茶可分为2类,其中S10,S2,S3,S7与 S1聚为一类,其他品种绿茶聚为一类。
2.6 绿茶对羟自由基清除作用和聚类分析
不同品种绿茶清除羟自由基能力和聚类分析见 图6。
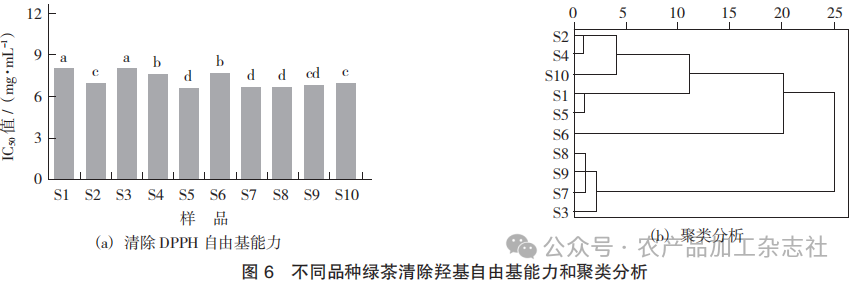
由图 6(a)可知,不同品种绿茶对羟自由基的 抑制活性不同。S5 清除羟自由基的作用最大,IC50 值为6.57 mg/mL。由图6(b)可知,当欧式距离平方 和为 10 时,10 种绿茶可分为 4 类,其中 S6 单独为一类,S2,S4 与S10 聚为一类,S1与 S5聚为一类,S7,S9,S8 与S3聚为一类。
2.7 绿茶多酚质量分数和聚类分析
不同品种绿茶多酚质量分数和聚类分析见图 7。
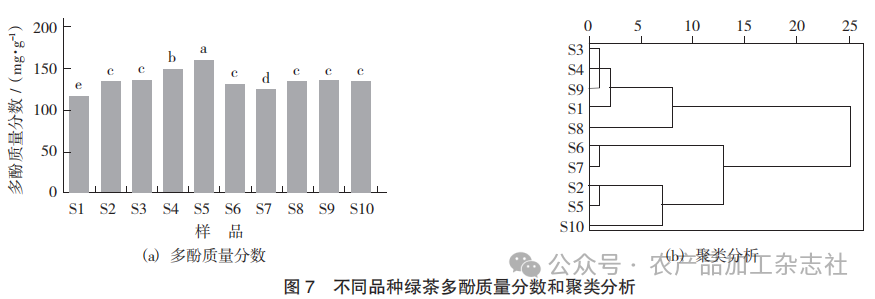
由图 7(a)可知,不同品种绿茶总多酚质量分 数为118.49~160.71 mg/g,S5多酚质量分数最高,且与其他产地绿茶比较具有显著性差异。由图 7(b) 可知,当欧氏距离平方和为10时,绿茶可分为3类, 其中S3,S4,S9,S1与S8聚为 一类,S6与S7聚为一类,S2,S5与S10聚为一类。
2.8 绿茶黄酮质量分数和聚类分析
不同品种绿茶多糖质量分数和聚类分析见图9。
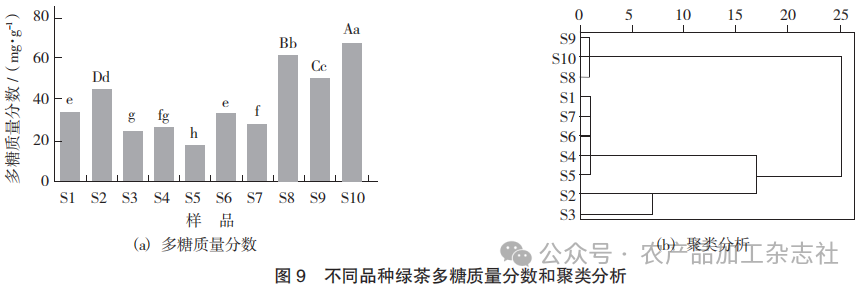
由图9(a)可知,不同品种绿茶粗多糖质量分 数为17.48~67.78 mg/g,多糖质量分数最高的是S10,最低的是S5,二者质量分数相差3倍多,且具有显著性差异。这可能与绿茶的生长环境(如气候、土 壤、日照等因素)有关。新疆日照时间最长,多糖 质量分数最高。由图9(b)可知,当欧氏距离平方和等于10时,10 种绿茶可分为3类,其中S8,S9 与S10聚为一类,S2与S3聚为一类,S1,S4,S5,S6 与S7聚为一类。
2.10 绿茶浸出物质量分数和聚类分析
不同品种绿茶浸出物质量分数和聚类分析见图10。
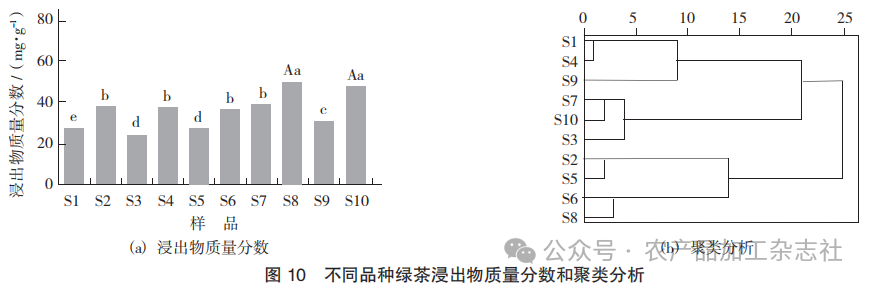
由图10(a)可知,不同品种绿茶浸出物质量分 数为30.38~62.79 mg/g,其中S8,S10的质量分数较高,且与其他地区绿茶的浸出物比较具有显著性差异。
由图10(b)可知,当欧氏距离平方和为10 时,10种绿茶分为4类,其中S1,S4与S9 聚为一类、 S10,S7与S3聚为一类,S2与S5聚为一类,S6与S8聚为一类。
2.11 相关性分析
绿茶抗氧化能力与化学成分、浸出物之间的相 关性热图见图 11。
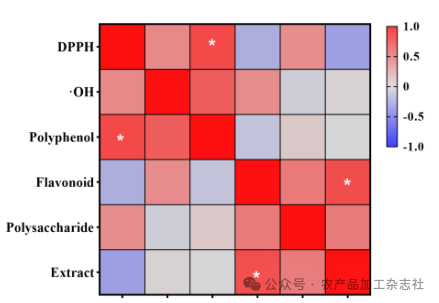

由图11可知,绿茶对DPPH自由基清除能力与多酚呈显著强正相关(p<0.05),相关系数为0.712,与多糖呈现较强正相关,与黄酮和浸出物呈现负相 关,但均无统计学意义,推测多酚可能是绿茶清除 DPPH 自由基的主要有效成分。绿茶对羟自由基清除能力与多酚、黄酮及浸出物均呈现正相关,与多糖呈现微弱负相关,但无统计学意义。
相关性分析表明,绿茶多酚、黄酮、多糖类成分都具有抗氧化功能,但抗氧化途径和机制不同,推测多酚可能是绿茶抗氧化作用的主要有效成分。
3 讨论
采用DPPH自由基和羟自由基的清除法评价绿茶的抗氧化能力,以DPPH自由基清除率为指标,通过单因素试验和正交试验法优选绿茶的浸泡工艺。结果表明,浸泡温度和浸泡时间对绿茶抗氧化性具有显著影响,最佳提取工艺为浸泡温度90 ℃,浸泡时间25 min,料液比1∶30(g∶mL)。该提取工艺简单可行,可用于绿茶抗氧化物质的制备。试验以绿茶抗氧化能力而非传统的感官分析、提取率或茶多酚含量进行提取工艺研究[29-31],结果与传统的绿茶冲泡法不同,说明在研究过程中应根据研究目标选择适宜的提取条件和筛选指标。研究结果亦为日常科学饮茶提供参考,为获得较强的抗氧化、抗衰老保健效果,饮茶时不宜用开水冲泡,浸泡时间不宜太长。
研究了10种不同品种绿茶的体外抗氧化能力。 结果表明,湖南武当绿茶与海南白沙绿茶抗氧化作用较强。因此,以抗氧化性保健效果考虑,武当绿茶和白沙绿茶品质较好,为日常保健饮用优选绿茶。相关性分析表明,多酚可能是绿茶清除DPPH自由基的主要活性成分。
分析了优选提取条件下10种不同品种绿茶的多 糖、多酚、黄酮及浸出物质量分数。结果表明,多酚质量分数最高的是桂林清明毛尖,最低的是贵州都匀毛尖;黄酮质量分数最高的是海南白沙绿茶,最低的是新疆叶尔羌;多糖质量分数最高的是新疆叶尔羌,最低的是桂林清明毛尖;浸出物质量分数最高的是海南白沙绿茶,最低的是贵州都匀毛尖,说明不同品种绿茶功能性成分质量分数差异比较大。
4 结论
采用体外抗氧化试验方法初步研究了10种不同 产地不同品种绿茶的三大类活性成分和抗氧化能力,结果表明,生态环境和品种对绿茶的次生物质代谢和抗氧化能力影响较大。为发挥绿茶应有的药效和食疗保健价值,应优先选择湖南武当绿茶和海南白沙绿茶。对于不同地区绿茶体内抗氧化效果和单体化学物质组成差异,有待今后进一步研究。
参考文献:
[1] 尹军峰,许勇泉,张建勇,等. 茶饮料与茶食品加工研 究“十三五” 进展及“十四五” 发展方向 [J] . 中国茶 叶, 2021, 43 (10) 18-25.
[2]TAMILSELVI E, ANBURAJ J, HARIPRIYA D, et al. Influence of shading intensity on chlorophyll, carotenoid and metabolites biosynthesis to improve the quality of green tea: A review [J] . Energy Nexus, 2023 (12): 100241-100255.
[3]张雪寒, 潘波旭, 宋勤飞, 等. 7 种贵州名优绿茶品质化 学成分分析 [J] . 食品安全质量检测学报, 2022(16): 5105-5111.
[4]DONG S, WU S, LI L, et al. Alleviation of lipid metabolic dysfunction through regulation of intestinal bacteriophages and bacteria by green tea polyphenols in Ob/Ob
mice [J] . Food Chemistry, 2024 (456): 139988-139996.
[5]周方,欧阳建,黄建安,等. 茶多酚对肠道微生物的调节作用研究进展 [J] . 茶叶科学, 2019, 39 (6): 619-630.
[6]LI M, QU R, LI P, et al. Green tea polyphenols reduced Porphyromonas gingivalis virulence and ameliorated aggra-vated gut inflammation by improving immunity and gut mi-crobiota dysbiosis [ J] . Food Bioscience, 2024 (60) :104519-104528.
[7]LV L, SHU H Y, MO X Y, et al. Activation of the Nrf2 antioxidant pathway by Longjing green tea polyphenols in mice livers [J] . Natural Product Communications, 2022,17 (12): 39409-39421.
[8]LV H, WANG J, GENG Y, et al. Green tea polyphenols inhibit TBBPA-induced lung injury via enhancing antioxidant capacity and modulating the NF-κB pathway in mice [J] . Food & Function, 2024 (39): 480-492.
[9]MHATRE S, SRIVASTAVA T, NAIK S, et al. 绿茶和红茶多酚类化合物的抗病毒活性在新型冠状病毒肺炎预防和治疗中的应用 [J] . 中国茶叶, 2021, 43 (1): 1-9.
[10]JAFARZADEH E, MOHSENI S H, KHANAVI M, et al. Exploring the synergistic effect of sildenafil and green tea polyphenols on breast cancer stem cell-like cells and their parental cells: A potential novel therapeutic approach [J] . Anti-Cancer Agents in Medicinal Chemistry, 2024, 24(4):304-315.
[11]何若菡,孙蕾蕾,王浩田,等. 茶多酚抗肥胖作用研究进展 [J] . 茶叶学报, 2022, 63 (2): 120-126.
[12]张姝萍,王岳飞,徐平. 茶多酚对动脉粥样硬化的预防作用与机理研究进展 [J] . 茶叶科学, 2019, 39 (3):231-246.
[13]张媛婷,夏艺菲,何晓琦,等. 绿茶和白茶中茶多酚提取工艺优化及抗氧化活性比较 [J] . 茶叶通讯, 2021,48(3): 507-513.
[14]MYLNIKOV M A, POLUKONOVA V N, ISAEV S D, et al. Identification of pathways of A498 human kidney carcinoma cell death under the action of Gratiola officinalis L. extract and green tea flavonoids using fluorescence imaging tech-niques [J] . Optics and Spectroscopy, 2020 (7): 972-979.
[15]YOO S, LEE Y, CHUNG J, et al. Enhancing the effect of catechins with green tea flavonol and polysaccharides on preventing lipid absorption and accumulation [J] . LWT, 2020(134): 110032-110047.
[16]陈洁静,段雪琳,徐培康,等. 绿茶糖苷类黄酮对酒精肝纤维化小鼠肝组织及肝功能的影响 [J] . 广西中医药,2019,42 (2): 35-38.
[17]钟旭为,尹茹琪,江名. 三种广西不同地区绿茶中总黄酮的提取及其抗氧化活性研究 [J] . 中国酿造, 2024,43(5): 180-184.
[18]WU B, XIAO X, LI S, et al. Transcriptomics and metabonomics of the anti -aging properties of total flavones of epimedium in relation to lipid metabolism [J] . Journal of Ethnopharmacology, 2018 (229): 73-80.
[19]张轶斌,刘鹏,纪海玉,等. 绿茶多糖提取工艺优化及其抗氧化活性分析 [J] . 食品工业科技, 2022, 43 (20):220-227.
[20]MA Y, XIE H, XU N, et al. Large yellow tea polysac-charide alleviates HFD-induced intestinal homeostasis dys-biosis via modulating gut barrier integrity, immune responses, and the gut microbiome [J] . Journal of Agricultural and Food Chemistry, 2024 (10): 616-633.
[21]ZHANG X G, LI Q N, HAN N, et al. Effects of Fu brick tea polysaccharides on gut microbiota and fecal metabolites of HFD/STZ-induced type 2 diabetes rats [J] . Food & Function, 2023 (29): 4215-4228.
[22]KUANG D D, LI Y X, QIAN P X, et al. Tea polysaccha-ride ameliorates high-fat diet-induced renal tubular ectopic lipid deposition via regulating the dynamic balance of lipo-genesis and lipolysis [J] . Journal of Agricultural and Food Chemistry, 2024 (21): 2606-2623.
[23]ZHOU A L, ZHOU C, LIU M J, et al. Anticancer effects of Camellia nitidissima Chi polysaccharide on hepatocellular carcinoma cells via apoptosis [J] . Journal of Herbal Medicine, 2023 (42): 100800-100818.
[24]HUANG R, YU H. Extraction methods, chemical compo-sitions, molecular structure, health functions, and poten-tial applications of tea polysaccharides as a promising bio-material: A review [J] . International Journal of Biological Macromolecules, 2024 (3): 134150-134165.
[25]邵郅胜,杨波,朱成,等. 不同生长阶段欧李叶片酚类物质含量及其抗氧化性 [J] . 西北植物学报, 2022, 42 (10):1720-1727.
[26]叶苗云,俞莉,白光剑,等. 黄芩多糖提取、 纯化方法筛选及优化 [J] . 江西中医药, 2024, 55 (5): 63-67.
[27]吕平. 陈皮与普洱茶总黄酮的协同抗氧化作用研究 [J] .食品研究与开发, 2020, 41 (3): 59-64.
[28]段宙位,陈婷,陈龙,等. 益智仁壳多酚不同提取工艺优化及其提取物的抗氧化性比较 [J] . 食品科技, 2021,46 (4): 180-187.
[29]张小琴,罗金龙,李燕,等. 不同造型白化绿茶滋味化学成分及感官品质分析 [J] . 南方农业学报, 2024, 55 (3):855-864.
[30]坤吉瑞,闫敬娜,舒娜,等. 不同日晒技术对晒青绿茶中挥发性化合物、 脂肪酸和感官品质的影响 [J] . 食品与发酵工业, 2020, 46 (21): 154-160.
[31]刘淑文,游静萍,李云冰,等. 影响茶叶中茶多酚含量的因素分析 [J] . 福建茶叶, 2022, 44 (2): 18-21.◇
编辑:谷金星
审核:关 颖
本篇文章刊登于《农产品加工》2026年2期上